A través de un proyecto de resolución, el Ministerio de Salud ha presentado cambios a los presupuestos máximos para la gestión y financiación de los servicios y tecnologías en salud no financiados con recursos de la Unidad de Pago por Capitación -UPC y no excluidos de la financiación con recursos del Sistema General de Seguridad Social en Salud -SGSSS. El documento, de ser aprobado, sustituiría la Resolución 586 de 2021.
Los ajustes del Ministerio de Salud a los presupuestos máximos aplicarán a las Entidades Promotoras de Salud – EPS en ambos regímenes, Entidades Obligadas a Compensar – EOC, Instituciones Prestadoras de
Servicios de Salud – IPS, operadores logísticos y gestores farmacéuticos, a la Administradora de los Recursos del Sistema General de Seguridad Social en Salud -ADRES y demás actores del sistema de salud colombiano.
De acuerdo con el proyecto de resolución, el presupuesto máximo de cada EPS o EOC será el resultado de la aplicación de la metodología que defina el Ministerio de Salud, la cual debe tener en cuenta la información consecutiva de doce (12) meses, como se hace según las disposiciones establecidas en la Resolución 586 de 2021.
También le puede interesar: Conozca los cambios a la Resolución 205 de 2020 sobre presupuestos máximos
Especificaciones sobre los servicios y tecnologías financiados con Presupuestos Máximos
Dentro de las modificaciones, el proyecto de resolución reajusta la descripción de los servicios y tecnologías, presentando detalles más concretos y quedando de la siguiente manera:
Medicamentos financiados con Presupuestos Máximos:
- Los medicamentos que ingresen al país, debidamente autorizados por el INVIMA, y tengan el mismo principio activo y forma farmacéutica de los medicamentos financiados con cargo al presupuesto máximo en las indicaciones autorizadas.
- Los medicamentos que se presentan en combinaciones de dosis fija que ingresen al país, que contengan principios activos autorizados. En todo caso, estas combinaciones cuando cumplan la regla de financiación con recursos de la UPC, serán financiadas con cargo a dicha fuente.
- Los medicamentos que contienen el metabolito activo de un principio activo o precursor financiado con cargo al presupuesto máximo, indistintamente de la forma farmacéutica, siempre y cuando tengan la misma indicación. Este criterio también aplica para medicamentos que no se encontraban incluidos en normas farmacológicas, y que luego de su autorización de ingreso al país se considerarán incluidos en el Presupuesto Máximo.
- Los medicamentos cuyo principio activo sea un estereoisómero de la mezcla racémica de un principio activo financiado con cargo al presupuesto máximo, siempre y cuando compartan el mismoefecto farmacológico del principio activo del cual se extraen, sin que sea necesario que coincidan en la misma sal o éster en caso de tenerlos. Este criterio también aplica para medicamentos que no se encontraban incluidos en normas farmacológicas, y que luego de su autorización de ingreso al país se considerarán incluidos como PM.
- Los medicamentos para el tratamiento de enfermedades huérfanas que venían garantizando la EPS o EOC al paciente con diagnostico confirmado en vigencias anteriores, y que no se encuentren financiados con recursos de la UPC.
- Los medios de contraste que no se encuentran financiados con recursos de la UPC.
- Los medicamentos diferentes a medios de contraste cuando sean usados para realizar pruebas farmacológicas diagnósticas y otros procedimientos diagnósticos financiados con cargo a estos recursos.
- Los medicamentos que actúen como estímulo in vivo o in vitro requeridos en un procedimiento incluido dentro de la financiación del presupuesto máximo, siempre y cuando sea necesario e insustituible para la realización de dicho procedimiento.
También le puede interesar: Regionalización sanitaria, política de acceso y Atención Primaria en Salud
- Los medicamentos nuevos incluidos en normas farmacológicas en el país que no sean financiados con recursos de la UPC.
- Los usos autorizados en la lista UNIRS de un medicamento financiado con cargo al Presupuesto Máximo y los que cumplan con lo estipulado en el parágrafo 3 del artículo 37 de la Resolución 2292 de 2021, o la norma que la modifique o sustituya.
- Los medicamentos clasificados por el INVIMA como Vitales No Disponibles y los prescritos por urgencia clínica según el Decreto 481 de 2004 o la norma que la modifique o sustituya, cuya autorización de importación fue otorgada por el INVIMA, que tengan definido un valor de referencia.
- Los medicamentos cuya financiación se define en el presente acto administrativo con cargo al presupuesto máximo, cualquiera sea el origen, forma de fabricación, el mecanismo de producción del principio activo, incluyendo la unión a otras moléculas que tengan como propósito aumentar su afinidad por órganos blanco o mejorar sus características farmacocinéticas o farmacodinámicas sin modificar la indicación autorizada.
- Las preparaciones derivadas del ajuste y adecuación de concentraciones de medicamentos incluidos en el presupuesto máximo o de la adecuación de estos en preparaciones extemporáneas o formulaciones magistrales, independientemente del nombre comercial del medicamento.
También le puede interesar: Reasignan recursos a línea de crédito con tasa compensada para EPS e IPS
¿Cuáles serán los procedimientos y APME financiados con Prespuestos Máximos?
- Los procedimientos en salud, que cumplan las siguientes condiciones: i) prescritos por un profesional en salud autorizado o sea ordenado por un fallo de tutela u orden judicial, ii) descritos en la Clasificación Única de Procedimientos en Salud – CUPS iii) que no se encuentren incluidos en la Resolución 2292 de 2021, las normas que las modifiquen o sustituyan y iv) que se prescriba a través de la herramienta tecnológica MIPRES.
También se entienden financiados los radiofármacos, así como los procedimientos de analgesia, anestesia y sedación, y por lo tanto los medicamentos anestésicos, analgésicos, sedantes, relajantes musculares de acción periférica y reversores de estos, que se consideren necesarios e insustituibles para la realización de un procedimiento financiado con cargo al presupuesto máximo. - En caso de que se requiera prestar de manera combinada, simultánea o complementaria procedimientos financiados con recursos de la UPC y financiados con Presupuesto Máximo, para cada uno se mantendrá la fuente de financiación definida.
No olvide leer: Presentan lineamientos para el programa de atención a víctimas – PAPSIVI
- Los injertos necesarios para los procedimientos contenidos en el presente acto administrativo, bien sean autoinjertos, aloinjertos, injertos heterólogos u homólogos. La financiación también incluye los procedimientos de toma de tejido del mismo paciente o de un donante.
- Los tratamientos reconstructivos no financiados con recursos de la UPC en tanto tengan una finalidad funcional, de conformidad con el criterio del profesional en salud tratante.
- Los estudios realizados a donantes no efectivos de aquellos trasplantes financiados con recursos de la UPC.
- Las tecnologías en salud oral no financiados con recursos de la UPC y que no sean procedimientos estéticos. También se entienden financiadas la anestesia general o sedación asistida de acuerdo con el criterio del profesional tratante.
- Las reintervenciones relacionadas con un procedimiento o intervención financiada con recursos de Presupuestos Máximos, conforme con la prescripción del profesional tratante.
En cuanto a los APME, serán financiados con Prespuestos Máximos los siguientes:
- Los productos para soporte nutricional clasificados como Alimentos para Propósitos Médicos Especiales – APME.
- El APME financiado con cargo al Presupuesto Máximo , deberá cumplir las siguientes condiciones para su prescripción: i) estar registrado ante el INVIMA con su respectiva clasificación como alimento para propósitos médicos especiales; ii) contar con concepto favorable vigente como APME, emitido por la Comisión Revisora de la Sala Especializada de Alimentos y Bebidas del INVIMA; y iii) que los dos requisitos anteriores hayan sido validados por el Ministerio de Salud y Protección Social antes de habilitar el producto en las tablas de referencia de la herramienta tecnológica MIPRES.
Por otra parte, los servicios complementarios prescritos por profesional de la salud autorizado u ordenados por autoridad competente, prestados por la red de prestación de servicios de salud de la EPS o EOC, de conformidad con la tabla de referencia de la herramienta tecnológica MIPRES.
La financiación de los medicamentos no financiados con recursos de la UPC cuya indicación sea específica y única para el tratamiento que requieran las personas que sean diagnosticadas por primera vez con una enfermedad huérfana durante la vigencia del presupuesto máximo será asumida por la ADRES, entidad que se mantiene como encargada del procedimiento de recobro/cobro el valor del tratamiento
farmacológico; el reconocimiento y pago de los medicamentos teniendo en cuenta los precios regulados (PRI) por la Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos – CNPMDM y los reportes respectivos.
Le puede interesar: “Decisiones Acertadas”: una iniciativa por la calidad en las decisiones clínicas
¿Cuáles servicios y tecnologías no estarán financiados por Presupuestos Máximos?
- Los servicios y tecnologías en salud financiados con recursos de la UPC, de riesgos laborales, de salud pública, y de otras fuentes, en consideración a que ya cuentan con su propia financiación.
- Los medicamentos clasificados por el INVIMA como Vitales No Disponibles y los prescritos por urgencia clínica según el Decreto 481 de 2004, cuya autorización de importación fue otorgada por el INVIMA, que no tengan definido un valor de referencia.
- Los medicamentos adquiridos a través de compra centralizada según determinaciones del Ministerio de Salud.
- Los medicamentos destinados al tratamiento de la indicación única para infección del SARS- COV-2/COVID-19 autorizados por el INVIMA.
- Los medicamentos cuya indicación sea específica y única para el tratamiento de una enfermedad huérfana, que no se encuentren financiados con recursos de la UPC, y que requiera la persona diagnosticada por primera vez durante la vigencia del presupuesto máximo.
- Los servicios y tecnologías expresamente excluidos de la financiación con cargo a recursos públicos asignados a la salud, definidos por la Resolución 2273 de 2021 o la norma que la modifique o sustituya, o aquellos que cumplan alguno de los criterios establecidos en el artículo 15 de la Ley 1751 del 2015, salvo los ordenados por autoridad judicial.
- Los servicios complementarios que no estén asociados a una condición en salud y que no sean prescritos por profesional de la salud, autorizados u ordenados por autoridad competente, o que por su naturaleza deban ser cubiertos por fuentes de financiación de otros sectores, o que correspondan a los determinantes en salud de conformidad con el artículo 9 de la Ley 1751 de 2015.
Los cambios que trae el proyecto de resolución, también recaen sobre las responsabilidades generales de las entidades e instituciones mencionadas al inicio del artículo. Aunque no se modifican en su totalidad, presentaremos las novedades a continuación:
No olvide leer: Hallan irregularidades en giros de la ADRES a prestadores por reclamaciones de accidentes de tránsito sin SOAT
Responsabilidades de las EPS y EOC
- Garantizar en forma integral tanto los medicamentos, APME, procedimientos de salud y servicios complementarios financiados con cargo a los recursos Presupuesto Máximo, como el conjunto de los servicios y tecnologías en salud financiados con recursos de la UPC, para el efecto establecerán modelos de atención y gestión, adoptarán en conjunto con los actores del sistema las guías o protocolos de atención que disponga este Ministerio. En caso de no estar al menos uno de estos documentos disponible, desarrollarán guías o protocolos de atención basadas en la evidencia nacional e internacional.
Los servicios y tecnologías en salud deben ser garantizados de manera efectiva, oportuna, ininterrumpida y continua, tanto al paciente hospitalizado, como al ambulatorio, de conformidad con el criterio del profesional de la salud tratante, absteniéndose de limitar, restringir o afectar el acceso a los servicios y tecnologías en salud. - Garantizar que todas las actividades y procesos propios del servicio farmacéutico, que implique servicios y tecnologías en salud financiadas con cargo al Presupuesto Máximo, se realicen bajo las condiciones y criterios definidos por la normatividad vigente, y quE su funcionamiento se ajuste a la habilitación, autorización y vigilancia por la autoridad competente para tal fin.
Cuando un establecimiento farmacéutico, entidad o persona (entiéndase bajo esta denominación incluidos los operadores logísticos y los gestores farmacéuticos) realice cualquier actividad o proceso propio del servicio farmacéutico, deberá cumplir las disposiciones del Capítulo 10 del Decreto 780 de 2016, Único Reglamentario del Sector Salud y Protección Social, en lo correspondiente, o según la norma que lo modifique o sustituya. - Realizar el cierre del ciclo de garantía de suministro de MIPRES con celeridad, oportunidad y calidad del registro. Para el cálculo anual del reconocimiento del Presupuesto Máximo el cierre del reporte de información de la vigencia fiscal anterior se debe realizar a más tardar el 31 de marzo de la vigencia en la cual se está realizando el cálculo, con el fin de que el reconocimiento contenga todas las prestaciones realizadas durante la vigencia fiscal anterior, sin perjuicio de que exista proceso administrativo de intervención forzosa o liquidación de la EPS o EOC.
No olvide leer: Ya comenzó la Ideatón 2022: por la sostenibilidad financiera del sistema de salud colombiano
Nuevas responsabilidades para IPS, operadores logísticos y gestores farmacéuticos:
- Deberán realizar el registro y reporte de la prescripción, suministro y facturación en los módulos de la herramienta tecnológica MIPRES según les corresponda, conforme a los tiempos estipulados en la normatividad vigente o pactados en los acuerdos de voluntades que permitan el cumplimiento de las responsabilidades de las EPS o EOC, sin perjuicio de que exista proceso administrativo de intervención forzosa o liquidación de la EPS o EOC.
- Cumplir los tiempos establecidos para realizar la facturación en los términos de los artículos 615 y 616 del Estatuto Tributario, del Decreto 4747 de 2007, y las normas que lo sustituyan o modifiquen.
Es importante tener en cuenta que, el monitoreo del reporte de información del presupuesto máximo estará a cargo del Ministerio de Salud y Protección Social y se realizará con las prescripciones, suministro y facturación de los servicios y tecnologías en salud no financiados con cargo a la UPC reportados en la herramienta tecnológica MIPRES para cada EPS o EOC.
El reporte de información corresponderá a los servicios y tecnologías en salud prestados durante la vigencia corriente, el cual se realiza de forma continua en el módulo de suministro de la herramienta tecnológica MIPRES. Los cortes de información de cada año corresponderán a:
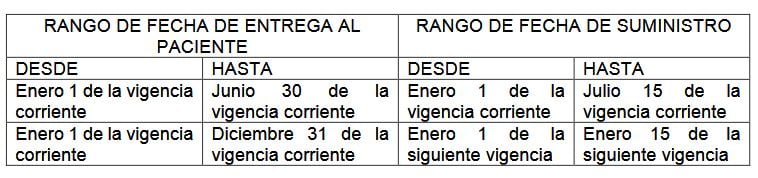
Consulte el proyecto de resolución que se encuentra anexo a este artículo:
Le puede interesar: BioSummit: biosimilares, una oportunidad para el sistema de salud colombiano






















