Durante décadas, la N-acetilcisteína (NAC) se ha reconocido como uno de los fármacos más eficaces contra infecciones virales de diversa índole. Hoy en día, su nombre ha cobrado especial relevancia con la pandemia, ya que su efectividad es objeto de estudio en pacientes que presentan la sintomatología respiratoria propia de COVID-19 en etapas avanzadas. Tales investigaciones, a su vez, se derivaron de estudios previos sobre la eficacia de la N-Acetilcisteína en otras enfermedades respiratorias, no relacionadas con el Sars-Cov-2.
El país no se ha quedado atrás con los avances investigativos. A inicios de 2020, Zambon Colombia SA, filial de Zambon SpA, realizó un exhaustivo metaanálisis titulado “ Eficacia y seguridad del uso de N-acetilcisteína parenteral en el manejo de los pacientes con síndrome de dificultad respiratoria del adulto (SDRA)”, con el apoyo del Grupo Proyéctame, centrado en el uso de NAC en pacientes con síndrome de distrés respiratorio agudo, posteriormente reconocido por la comunidad médica internacional como el indicio más común en individuos con COVID-19 en etapa avanzada.
El desarrollo de SDRA, al igual que en otras patologías, depende de la respuesta inmunitaria de cada organismo. Ante una baja o media respuesta, se desencadenan en el organismo 3 procesos fundamentales: sobreproducción de moco, respuesta inflamatoria exagerada -tormenta de citoquinas-, coagulopatías y endoteliopatías. Los fenómenos son idénticos a los presentados por los afectados por COVID-19, producto de la respuesta del proceso inflamatorio que el virus genera en el cuerpo humano.
El tapón mucoso, debido a la infección, bloquea las vías aéreas e impide el paso del aire. Cuando se trata de infectados con Sars-Cov-2, este cambia totalmente su consistencia por una más espesa y viscosa que termina por adherirse completamente a los tejidos. A su vez, la tormenta de citoquinas, causante de sepsis, se sugiere como otro de los efectos propios de la nueva enfermedad, producto de la replicación sostenida del virus.
De acuerdo con una investigación sobre este tema, publicada en Cell Press, el exceso de citoquinas encaja con los modelos de inducción antiviral convencional, pero se desconoce si la hiperactividad inmunológica o la falta de resolución en la respuesta inflamatoria -consecuencia de la replicación del virus- subyacen a la enfermedad grave. Sin embargo, los informes presentados por la comunidad médica, revelan aumentos en la formación de trombos y muerte de células endoteliales en afectados por COVID-19, el último proceso característico mencionado previamente.
En el metaanálisis realizado por Zambon Colombia SA en pacientes no Covid con SDRA , bajo el modelo AMSTAR, se seleccionó la siguiente evidencia médica:
Fuente original: Metaanálisis realizado por Zambon Colombia SA.
Los resultados evidenciaron que los efectos mucolíticos, antioxidantes y antiinflamatorios producen una respuesta más efectiva cuando se administra parenteralmente a pacientes críticamente enfermos (UCI). La N-acetilcisteína como mucolítico disuelve la densidad del moco producido en exceso, rompe el tapón mucoso alojado en las vías respiratorias y por ende, posibilita su expectoración y facilita el paso de aire. Si se trata del efecto antioxidante, actúa directamente sobre TNFa, IL-1, IL-6 e IL-8; disminuyendo las citoquinas proinflamatorias generadas durante el síndrome y, finalmente, reduce la agregación plaquetaria y los trombos arteriales gracias al efecto antitrombótico del medicamento.
Al utilizarse la NAC como fármaco coadyuvante, en el metaanálisis se comprobó que uso de N-Acetilcisteína intravenoso en dosis de 200 mg por kg por día por al menos 5 días, reduce en 18.4% la estancia en UCI; es decir, se acorta la permanencia en las unidades de cuidado intensivo en 4.47 días.
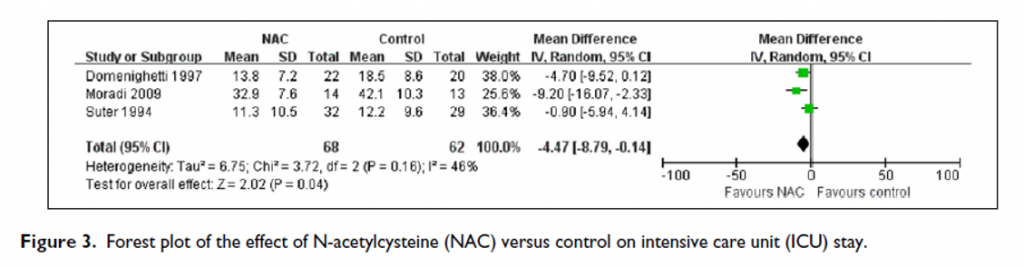
Fuente original: “Metaanálisis de Lu” integrado en el metaanálisis de Zambon Colombia SA.
Debido a que el medicamento no interviene directamente en los agentes causantes del SDRA, no se puede considerar como un tratamiento generalizado para el síndrome. Aunque se destaca su alto perfil de seguridad, no se detectó una reducción significativa en los niveles de mortalidad asociados al uso de N-acetilcisteína en estas circunstancias particulares. Es decir, como medicamento adyuvante en el manejo integral del síndrome en UCI.
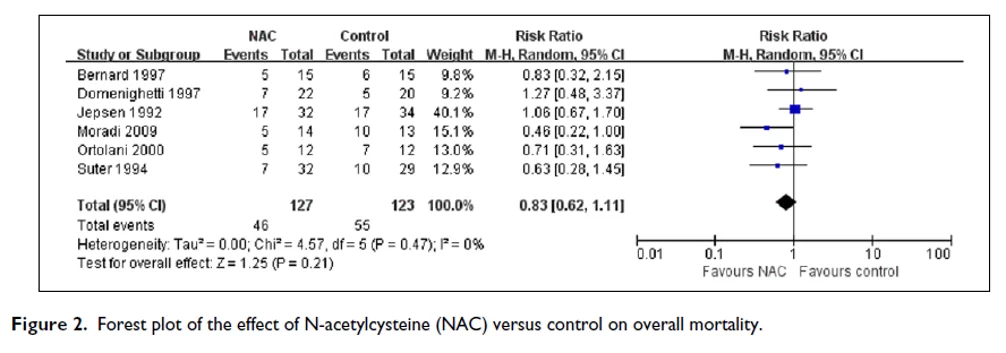
Fuente original: “Metaanálisis de Lu” integrado en el metaanálisis de Zambon Colombia SA.
Evidencias adicionales apuntan al mismo resultado
Desde que la OMS anunció la pandemia provocada por Sars-Cov-2, el 11 de marzo, la comunidad médica y científica busca desesperadamente una cura definitiva. En el proceso, se ha seleccionado a la N-Acetilcisteína en estudios sobre COVID-19 adelantados en más de 19 países entre los que se incluyen EE.UU., Inglaterra, España, Rusia y China.
En abril, un mes después de completado el metaanálisis de Zambon Colombia SA y primer mes de pandemia, el British Medical Journal (BMJ) publicó un metaanálisis y revisión sistemática sobre el uso de agentes mucoactivos para la insuficiencia respiratoria aguda en pacientes críticamente enfermos, entre los que se incluye la administración de NAC por vía intravenosa y NAC en nebulización. El análisis se concentró en 5 aspectos concretos -además de la revisión de la literatura científica elegida y la evaluación del riesgo-: duración del uso de ventilación mecánica, duración en UCI, duración de estancia hospitalaria, días sin uso de ventilador y mortalidad.
- Duración del uso de ventilación mecánica: se reportó el uso de estas herramientas en 7 ensayos de los analizados (n=1226) pero no se evidenció ningún efecto positivo derivado de la administración de agentes mucoactivos de alta heterogeneidad.
- Días sin uso de ventilador: Según la información analizada, tres ensayos reportaron días sin ventilador: dos en el día 28 y uno en el día 30. Sin embargo, no se encontró ninguna diferencia sobre los días libres del aparato. Como nota aclaratoria, el grupo de expertos a cargo del metaanálisis mencionó que en un ensayo, la media de días libres de ventilador fue de 11 -en personas tratadas con agentes mucoactivos- vs. 3 días libres – en pacientes tratados con placebo. Pero no fue incorporado al metaanálisis porque no pudo determinarse la SD media.
- Estancia en el hospital: al igual que en los anteriores, se dice que no hubo ningún cambio significativo en la estancia hospitalaria. A la conclusión se llegó tras revisar la información presentada en cuatro estudios del metaanálisis.
El hallazgo más importante de este metaanálisis, respecto a la estadía en UCI, reafirma las conclusiones del elaborado por Zambon Colombia ZA. Ninguno compartió sus fuentes.
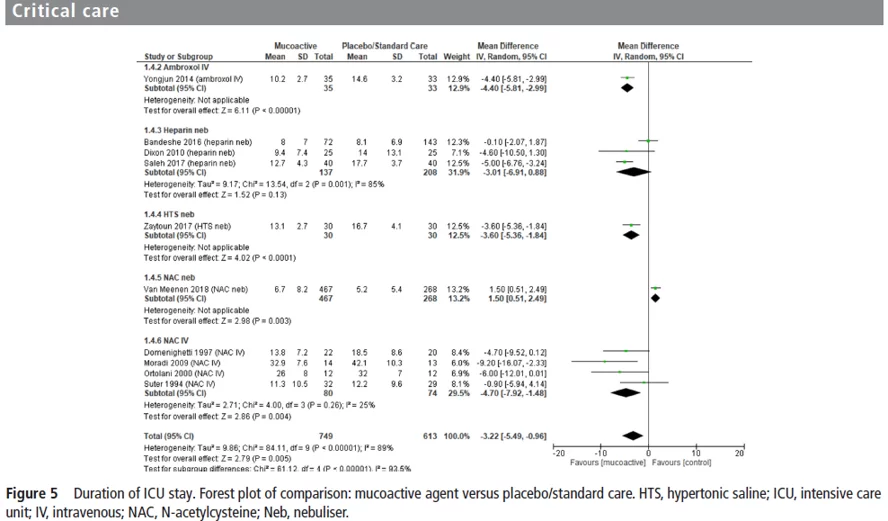
Fuente: Metaanálisis liderado por Ronald Anand, publicado en BMJ.
De acuerdo con la información presentada, la administración de N-Acetilcisteína por vía intravenosa redujo en 4.7 días la permanencia en la unidad de cuidados intensivos. El resultado es bastante cercano al obtenido por Zambon Colombia ZA pese a los distintos porcentajes de heterogeneidad I2 de cada uno. El estudio del BMJ presenta un I2 del 25% en comparación con el I2 del 44%, obtenido en el metaanálisis de la farmacéutica. Es decir, la ratificación de los resultados proviene de un estudio más preciso (publicado en BMJ).
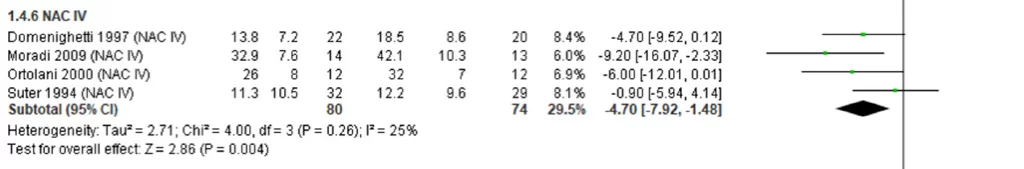
Fuente: Metaanálisis liderado por Ronald Anand, publicado en BMJ.
La mortalidad es el segundo aspecto que concuerda con el análisis hecho por Zambon Colombia SA. Sobre ello, los investigadores del análisis publicado en la revista británica afirman que los agentes mucoactivos no tienen ningún efecto sobre la mortalidad de los pacientes con insuficiencia respiratoria aguda. Al dividir la información en subgrupos, no se evidenció algún cambio producido por el uso de NAC intravenosa.
Vale la pena tener en cuenta que, dentro de la población estudiada por Anand, se incluyen a los individuos afectados con falla respiratoria hipóxica (tipo 1), falla respiratoria hipercápnica aguda (tipo 2), SDRA y lesión pulmonar aguda. Pero la evaluación de eficacia y seguridad para la N-Acetilcisteína se realizó solo con su uso en pacientes con SDRA. Debido a que este estudio se conoció posteriormente a la fecha de corte del realizado por Zambon Colombia, los investigadores locales no incluyeron los datos ya presentados.
¿Juega la NAC un rol fundamental en el tratamiento de pacientes con COVID-19?
En julio, la revista ELSEVIER presentó el artículo “Bloqueo terapéutico de la inflamación en una infección severa de COVID-19 con N-Acetilcisteína intravenosa” (nombre traducido al español), en el que se expone el caso clínico de un hombre de 44 años, tratado en Nueva York por COVID-19 al que inicialmente se le suministró una única dosis de hidroxicloroquina 400 mg, al día siguiente de haber sido hospitalizado y al que se le administró NAC por vía intravenosa 10 días después de su ingreso en el centro hospitalario, debido a que no manifestó ninguna mejoría y requirió una intubación.
Desde la primera aplicación, se evidenció una mejora inmediata en los índices de hemolísis. En una segunda ronda, se identificó la reducción sostenida de los niveles de bilirrubina como acción producida por el fármaco. Adicionalmente, los médicos que adelantaron el estudio notaron que los marcadores inflamatorios se redujeron drásticamente con el uso de NAC, aunque al mismo tiempo se le habían suministrado esteroides.
Al repetir el tratamiento con N-Acetilcisteína en 9 personas más, se observó una reducción general significativa de los marcadores inflamatorios (CRP, ferritina y Proporción Neutrófilo/linfocitos) durante la administración de la NAC por vía intravenosa. En 6 pacientes se observó un efecto rebote tras abandonar el tratamiento mientras que los 3 restantes no experimentaron efectos adicionales. Sin embargo, la conclusión fue la misma en todos los casos: el uso de NAC por vía intravenosa bajó considerablemente los marcadores de inflamación y permitió que los pacientes fueran dados de alta más rápido, debido a la mejoría notoria de sus síntomas.
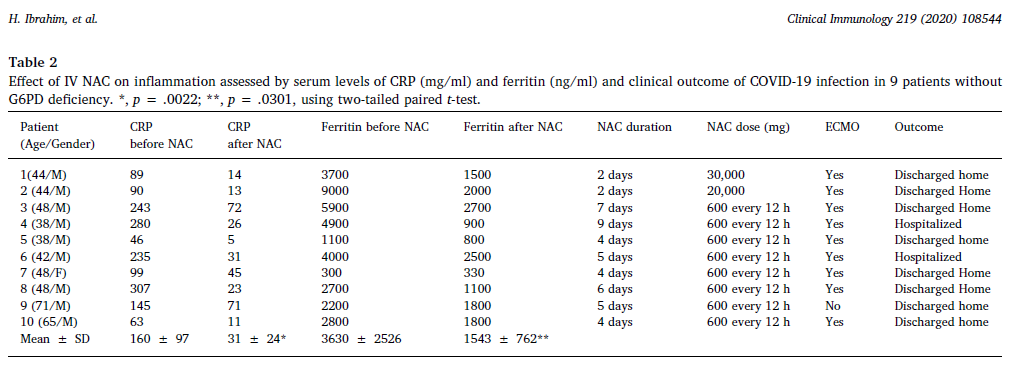
Fuente: Estudio “Bloqueo terapéutico de la inflamación en una infección severa de COVID-19 con N-acetilcisteína intravenosa”.
Esta tabla, documenta que a dosis de 30000 – 20000 mg por vía intravenosa, el paciente puede salir de UCI a los 2 días. Si se administra el fármaco en dosis menores a 200 mg/kg/ día, la estancia es prolongada. Los resultados aquí presentados soportan la viabilidad del uso de NAC a dosis altas, tal y como está documentado en el metaanálisis elaborado por Zambon Colombia SA.
Más recientemente, el 5 de agosto, se publicó en el Journal of Personalized Medicine el artículo “Postulated Adjuvant Therapeutic Strategies for COVID-19” en el que se mencionan algunas estrategias adyuvantes para COVID-19. El estudio se concentró en 12 agentes, elegidos por su mecanismo de acción farmacológica frente a una o varias entre 7 alteraciones que produce la infección por Sars-Cov-2: desregulación del sistema inmunológico, entrada del virus en las células sanas, replicación del virus, exagerada respuesta inflamatoria, estrés oxidativo, trombosis y daños en el endotelio.
Para evaluar la eficacia de los medicamentos seleccionados, se utilizó una clasificación previa que segmenta la evolución de COVID-19 en 3 fases, de acuerdo con la severidad de los síntomas que experimentan los individuos contagiados.
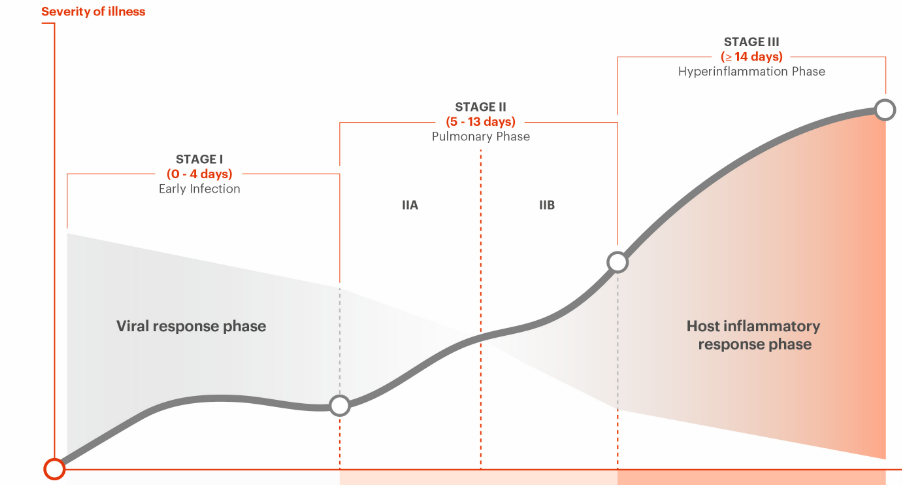
Fuente: Postulated Adjuvant Therapeutic Strategies for COVID-19 publicado en JPM.
El estadío II y III corresponden a las fases moderadas y avanzadas de la enfermedad. Aunque ya es conocido que entre el día 5 y 12 se desarrollan las complicaciones pulmonares, al mismo tiempo representa una ventana de 7 días que podrían hacer la diferencia en el proceso de recuperación. Como hasta hoy no hay guías clínicas establecidas, se corre el riesgo de que el virus madure y genere el proceso inflamatorio multisistémico del cual, miles de infectados no se recuperan.
Dentro de las principales complicaciones asociadas a COVID-19, el estudio incluye a la lesión pulmonar aguda (LPA) y al síndrome de distrés respiratorio agudo (SDRA), tema de atención en las investigaciones referidas anteriormente. Con base en ello, este equipo de expertos presenta una tabla con los fármacos recomendados como adyuvantes en el tratamiento actual. Para la N-Acetilcisteína se sugiere la administración de 560 mg, dividida en 3 dosis diarias (1 cada 8 hrs).
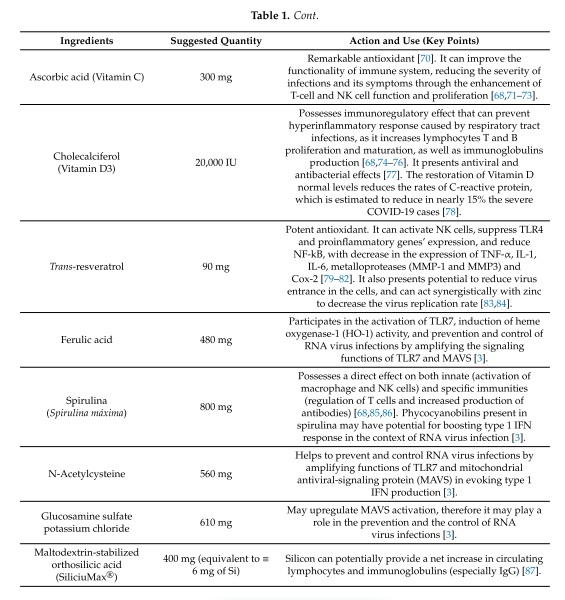
Fuente: Postulated Adjuvant Therapeutic Strategies for COVID-19 publicado en JPM.
Se identificaron los siguientes roles específicos para la N-Acetilcisteína en la infección por COVID-19:
- Reducción de la entrada del virus en la célula: La N-Acetilcisteína contiene el inhibidor DPP4R. Actualmente, se conoce que el ARNm de DPP4 y la expresión de la proteína están inversamente relacionados con la función pulmonar y los parámetros de capacidad difusora, lo que explicaría la propensión de los fumadores y personas con enfermedad pulmonar obstructiva crónica (EPOC) para desarrollar COVID-19.
- Activación del TLR7/ Respuesta al Interferón Tipo 1: Según la investigación, la N-Acetilcisteína podría contribuir en la prevención o control de las infecciones causadas por virus ARN, ya que el fármaco amplifica las funciones de señalización de TLR7 y la proteína mitocondrial de señalización antiviral (MAVS) en la producción de IFN tipo 1. Como se menciona en el artículo, los IFN logran inhibir la replicación del coronavirus tipo SARS así que pueden ser útiles en el tratamiento para COVID-19. Adicionalmente, la activación del TLR7 por el ARN viral de una sola hebra, atrapado dentro de los endosomas, proporciona un estímulo clave para la inducción de IFN de tipo 1 por el virus del ARN.
- Apoyo en la reducción del estrés oxidativo: el Sars-Cov-2 desencadena un mecanismo recurrente de infecciones virales: activa una respuesta pro-oxidante de los macrófagos a través de la estimulación de la TLR que da lugar a la activación del TNF-α del NADPH que, a su vez, media la producción de ROS. Para reducir los ROS se necesitan antioxidantes esenciales como el glutatión (GSH) y la glutatión peroxidasa (GPx) que neutralizan estas sustancias y las transforman en productos no tóxicos para el organismo. El uso de N-Acetilcisteína eleva la producción de glutatión, especialmente en personas mayores, puesto que los niveles del antioxidante y de la cisteína en el plasma disminuyen con la edad.
Aunque esta investigación no consideró el efecto mucolítico que destaca comúnmente a la N-Acetilcisteína, su uso antioxidante y antiinflamatorio es el más relevante. Es decir, puede ser utilizado como medida preventiva antes de que los síntomas de COVID-19 evolucionan desfavorablemente y conduzcan hacia una estancia en UCI o puede ser administrado en pacientes con mayor gravedad.
Si se habla de un panorama más general, la evidencia aquí presentada demuestra que los efectos de la N-Acetilcisteína favorecen el proceso de recuperación en todo tipo de pacientes. Sin embargo, no puede ignorarse que, la administración del fármaco -como soporte al manejo estándar- a quienes se encuentran en cuidados intermedios o intensivos produce una mejoría en su sintomatología que los aleja de los tratamientos invasivos y, por ende, minimiza las secuelas que éstos generan.
Tampoco puede pasarse por alto que, el uso de NAC disminuye los días de permanencia de los pacientes en UCI, abriendo la posibilidad a una atención de calidad y en menor tiempo a las personas que lo requieran, sin afectar la disponibilidad de camas o la infraestructura que tales unidades necesitan para su adecuado funcionamiento.
Actualmente, el país se rige por la guía metodológica colombiana para la elaboración de guías de práctica clínica (GPC), para emitir recomendaciones a los profesionales de la salud. Dentro de los requisitos establecidos, presentar evidencia científica de alta calidad es uno de los primordiales. Sobre este punto, se debe tener en cuenta que las revisiones incluidas en el metaanálisis de Colombia y las investigaciones adicionales realizaron la evaluación de calidad de los ensayos clínicos incluidos, mediante la herramienta de riesgo de sesgo de la colaboración Cochrane. Por ahora, el uso de la N-Acetilcisteína no está reglamentado como tratamiento coadyuvante, ni se le han dado otros usos distintos a los usuales, aprobados por el Invima.