CONSULTORSALUD conoció que a través de la resolución 8929 de 2019, la Empresa Mutual para el Desarrollo Integral de Salud, Emdisalud E.S.S. EPS-S, será liquidada totalmente, esto debido a las innumerables quejas e irregularidades en la prestación de los servicios de salud.
También puede leer: Cruz Blanca EPS sale del sistema
Se trata de la segunda intervención que ordena el superintendente de Salud en menos de una semana. De acuerdo a los argumentos expuestos por la entidad, desde el 2013 la situación financiera de está EPS ya se venía deteriorando. En este año, se encontraba bajo medida de vigilancia especial y su intervención se había prorrogado por acuerdos presentados con la Superintendencia de Salud para que la EPS subsanará y optimizará las operaciones derivadas del aseguramiento en salud.
A la EPS Emdisalud se le dieron plazos para que llevara a cabo planes de mejora que solventaran y corrigieran las desviaciones que se están presentando en el sector salud, asimismo, mitigara los riesgos financieros que estaba atravesando y pudiera finalmente cubrir obligaciones con terceros, conllevando a que la entidad en un menor tiempo mantuviera el punto de equilibrio.

Sin embargo, según el análisis presentado por la superintendencia Delegada de Medidas Especiales la situación financiera de la EPS presentaba deterioro año tras año, y sus pasivos eran superiores al activo en casi 5 veces.
“La situación financiera se ha venido deteriorando debido a que los pasivos de la entidad estaban aumentado significativamente, afectando la operación corriente y dando origen al desmejoramiento del patrimonio”. Indica el documento.
Lo que permite inferir que los indicadores de siniestralidad PBS a corte de marzo de 2019 fueron de 100,32%, siendo esta elevada, y reflejando las debilidades de la entidad en términos de contención del costo y optimización de ingreso por concepto de UPC, para corte a junio de este mismo año, sus activos fueron de $96.000 millones, sus pasivos $503.000 millones y adicionalmente presentaba patrimonio negativo de $-402.491 millones de pesos.
También puede leer: ¿será posible pensionarse en Colombia?
Situación que demuestra que la gestión administrativa en el manejo de los recursos de salud de Emdisalud han sido deficientes, generando un riesgo en el aseguramiento y en la gestión en salud de la población afiliada.
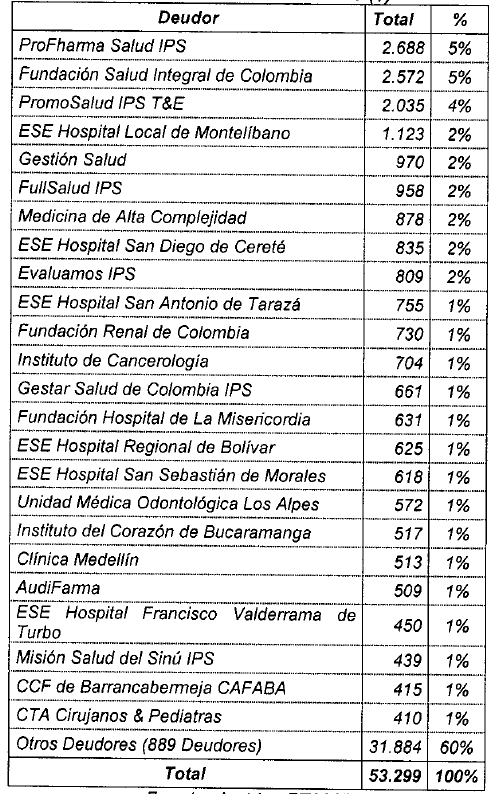
Concentración de Anticipos
El 40% de los Anticipos eran de ($21.415 millones) y estaban concentrados en 24 Prestadores de Servicios de Salud, los cuales se relacionan así:
Peticiones, Quejas, Reclamos, Denuncias (PQRD)
De otra parte, de acuerdo con denuncias conocidas y publicadas por CONSULTORSALUD, a la fecha Emdisalud tiene un promedio acumulado para el trimestre de 2019 de 49,56% de quejas por los incumplimientos en la cobertura de la prestación de sus servicios para baja y alta complejidad, en 2018 su reporte fue de 42,91% y según la Supersalud el estándar debe estar por debajo de 33,52%.
En tal sentido, entre las faltas que logró identificar la Supersalud están:
En lo técnico-científico
La cobertura de servicios de baja y alta complejidad en el territorio nacional es insuficiente, hechos que ponen en riesgo la vida y la salud de los afiliados.
Por ejemplo, a marzo de 2019, en cobertura de servicios básicos como atención en medicina general, promoción y prevención, consulta odontológica y laboratorio clínico no superan el 53%. Las unidades de cuidados intensivos para adultos solo alcanzan una cobertura del 61% y de solo el 23% en UCI pediátrica y neonatal.
Población Materna
La población materna (de alta vulnerabilidad en salud) no tiene la garantía de la prestación de los servicios. La cobertura en el territorio nacional para la atención en oncología, hematología, quimioterapia y radioterapia es del 0%, y, entre muchos otros aspectos, tampoco cumple con la entrega completa y oportuna de los medicamentos.
Desviación de indicadores en Enfermedad Renal Crónica
De igual manera, los hallazgos descritos en el documento muestran que Emdisalud presentaba desviación de los indicadores de seguimiento a Enfermedad Renal Crónica ERC de: Porcentaje de captación de hipertensión arterial (HTA) en personas de 18 a 69 años en régimen subsidiado 9.93%; porcentaje de captación de diabetes mellitus en personas de 18 a 69 años régimen subsidiado 18.70%”
En la respuesta emitida por la EPS indica que el número de pacientes a captaren el mes de enero es de 4897, lo cual difiere del resultado del hallazgo, siendo el valor real 1.200/0 de captación de
pacientes hipertensos de 18-69 años.


Experiencia de la Atención
Frente a esta evaluación de comportamiento, los indicadores de experiencia en la atención durante el año 2018 y el primer trimestre de 2019, en el promedio acumulado se puede evidenciar que la Empresa Mutual para el Desarrollo Integral de la Salud “EMDISALUD”, para diciembre de 2018 presento incumplimiento en 6 de los 16 indicadores objeto de seguimiento al plan de acción, los cuales no lograron durante el año 2018 cumplir con la meta establecida.
En lo financiero
Emdisalud no cumple con los parámetros de solvencia y liquidez. Tras 23 años de funcionamiento en el régimen subsidiado y 18 en el régimen contributivo, la EPS enfrenta más de 606 procesos judiciales, por ineficiencia en el pago de indemnizaciones, de perjuicios por incumplimientos de acuerdos de paso y demoras en pagos de facturación.
Esta entidad de salud opera en los departamentos de Antioquia, Bolívar, Boyacá, Cesar, Chocó, Córdoba, Magdalena, Santander y Sucre y de acuerdo al reporte de sus deudas, hasta marzo de este año tenía pendiente más de 50 cuentas por pagar, siendo Córdoba, donde se encuentra la base de su administración, en donde más deben.
También puede leer: llegó el reglamento del MAITE – resolución 2626 de 2019
Parte de tranquilidad a los afiliados
Finalmente, la Superintendencia Nacional de Salud, da un parte de tranquilidad a los afiliados a Emdisalud quienes según asegura la entidad, no se verán afectados con la medida. En consecuencia en los próximos días el Ministerio de Salud publicará el listado de las EPS que recibirán a los usuarios a partir del 1 de noviembre, prestadoras sobre las que la Supersalud no tiene medida de vigilancia especial alguna.
A ningún usuario se le interrumpirá el servicio. Emdisalud deberá garantizar la atención con normalidad hasta el 31 de octubre y desde el día siguiente, 1 de noviembre las EPS receptoras se harán cargo de los afiliados.


















