El Invima otorgó el primer registro sanitario para un medicamento biosimilar, soportado en estudios de comparabilidad, frente al producto innovador que mantenía el monopolio. Se trata del trastuzumab, un anticuerpo monoclonal, utilizado para cánceres, principalmente el de seno. Así lo señala una nota del El Tiempo.
El registro del trastuzumab
Por consiguiente, el registro fue otorgado al laboratorio Mylan-GMBH y será comercializado con el nombre de Ogivri y puesto a disposición del mercado colombiano, un gran avance ya que este producto tendrá un costo inferior al producido por el laboratorio original.
Cesar Burgos, Presidente de la Asociación Colombiana de Sociedades Científicas, explica que los medicamentos biotecnológicos son fármacos que se obtienen a partir de organismos vivos o tejidos, en los que las fuentes y métodos de producción incluyen cultivos de células de microorganismos o el uso de fluidos orgánicos como la sangre.
Principales usos
No obstante, dentro de los principales usos y aplicaciones de estos medicamentos, cuyas características son los elevados precios, están los más modernos tratamientos para el cáncer, la diabetes, la artritis, las hepatitis B y C y algunas enfermedades neurológicas o de la sangre.
Polémica por elaboración de biosimilares
Por otra parte, en el 2014, se firmó el decreto 1782 por el Presidente de la República y el Ministro de Salud de ese entonces, que buscaba para su aplicación normatizar la producción y comercialización de productos biotecnológicos y tener en cuenta la definición de los medicamentos biológicos que se enuncian como “medicamentos derivados de organismos o células vivas o sus partes” y que fueran obtenidas de fuentes como “tejidos o células, componentes de la sangre humana o animal”.
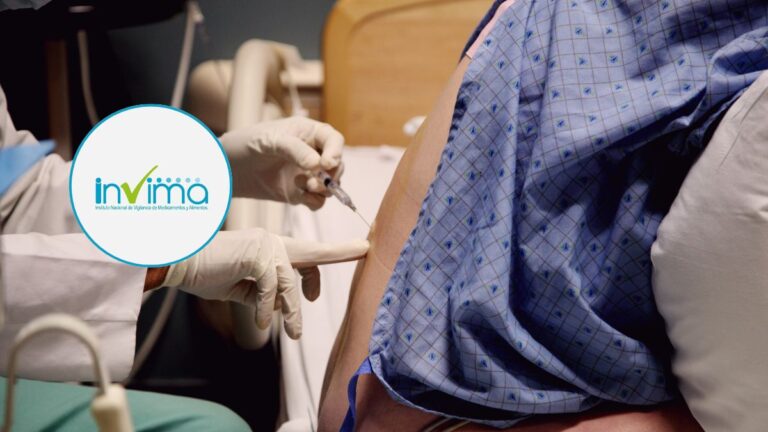
Bajo esta norma, se acaba de aprobar el Ogivri, que de acuerdo con el Director del Invima, Julio Cesar Aldana, está respaldado por rigurosos estándares de calidad y seguridad.
Precios elevados de los medicamentos en Colombia

“es preocupante que un colombiano no pueda acceder a un medicamento por su elevado precio, como que lo reciba de mala calidad”.
Así mismo, aldana dice que “es preocupante que un colombiano no pueda acceder a un medicamento por su elevado precio, como que lo reciba de mala calidad. De tal forma que en la aprobación de este producto y en todos los que se aprobarán, el Invima no ahorra esfuerzos para garantizar la máxima calidad de los productos, el seguimiento a sus efectos y su calidad y la exigencia de responsabilidades para los fabricantes”.
De igual manera menciona aldana, a la fecha el Invima ha analizado 154 solicitudes de registros sanitarios específicos para medicamentos biológicos, de los cuales se han otorgado siete registros en calidad de propios (innovadores) y uno solo, soportado bajo el concepto de biosimilaridad. Según un comunicado en curso, se encuentran 28 solicitudes de registro sanitario por la vía de la comparabilidad (biosimilares), de los cuales dos están en etapa de emisión de registro sanitario, también con el principio trastuzumab.