La Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos (CNPMDM) sometió en mayo de 2026 una segunda versión del proyecto de Circular 20 a consulta pública. El texto busca actualizar el precio máximo de venta de los medicamentos sujetos al régimen de control directo de precios aplicando la metodología establecida en la Circular 18 de 2024. La primera versión de este proyecto circuló en diciembre de 2025. Entre una versión y otra, cuatro mercados cambiaron de categoría, la tasa de cambio fue corregida y el número de mercados con precio modificado pasó de 23 a 40.Que el proyecto de Circular 20 haya requerido una segunda ronda de consulta pública no corresponde al procedimiento estándar. El Decreto 1081 de 2015 establece un único período de publicidad de 15 días hábiles para esta clase de actos administrativos de regulación de precios. La reapertura del proceso señala que los comentarios recibidos en diciembre de 2025 identificaron errores de fondo suficientes para que la Comisión decidiera corregirlos antes de expedir la norma.
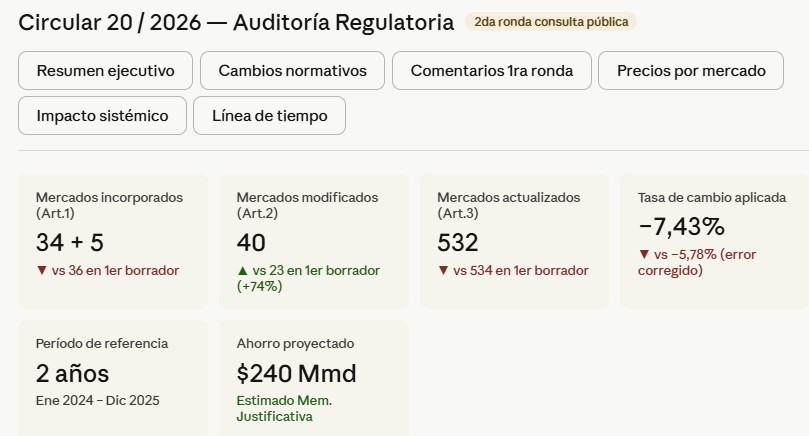
La tasa de cambio de −5,78% a −7,43%: el error de período y su corrección
El artículo 3 del proyecto actualiza los precios máximos de venta de los mercados relevantes ya bajo control directo aplicando la variación porcentual promedio de las tasas de cambio de los países de referencia, según lo establecido en el artículo 23 de la Circular 18 de 2024. El primer borrador calculó esa variación sobre el período enero–diciembre de 2024, lo que arrojó una tasa de −5,78%. El segundo borrador aplica el período enero 2024–diciembre 2025 y obtiene −7,43%.
El artículo 23 de la Circular 18 de 2024 establece que la actualización aplica “para el período comprendido entre la fecha de la última actualización y la fecha del cálculo”. La Circular 19 de 2024 —el último acto de actualización anterior— cubrió precios hasta diciembre de 2023. La Comisión inició la implementación de la Circular 18 de 2024 en enero de 2025 sin que durante ese año se expidiera un acto administrativo de actualización, situación que el propio segundo borrador reconoce textualmente en sus considerandos. El período correcto, por lo tanto, era de 24 meses, no 12.
La diferencia de 1,65 puntos porcentuales entre las dos tasas desplaza hacia abajo los precios máximos de venta de 532 mercados regulados en todas las transacciones: primaria institucional, primaria comercial, secundaria institucional y secundaria comercial. El margen de ajuste del 9,6%, calculado conforme al artículo 10 de la Circular 18 de 2024, no fue modificado.
El segundo borrador introduce además una distinción que la primera versión no contemplaba: diferencia entre la tasa de cambio que se usa para calcular el Precio de Referencia Internacional (PRI) —conforme al artículo 5 de la Circular 18 de 2024— y la tasa que aplica para actualizar los precios de mercados ya bajo control directo conforme al artículo 23. Ambas tasas corresponden a períodos distintos porque parten de momentos diferentes en la historia de cada mercado. Ese detalle técnico fue señalado por múltiples actores en la primera ronda y quedó incorporado en el texto.
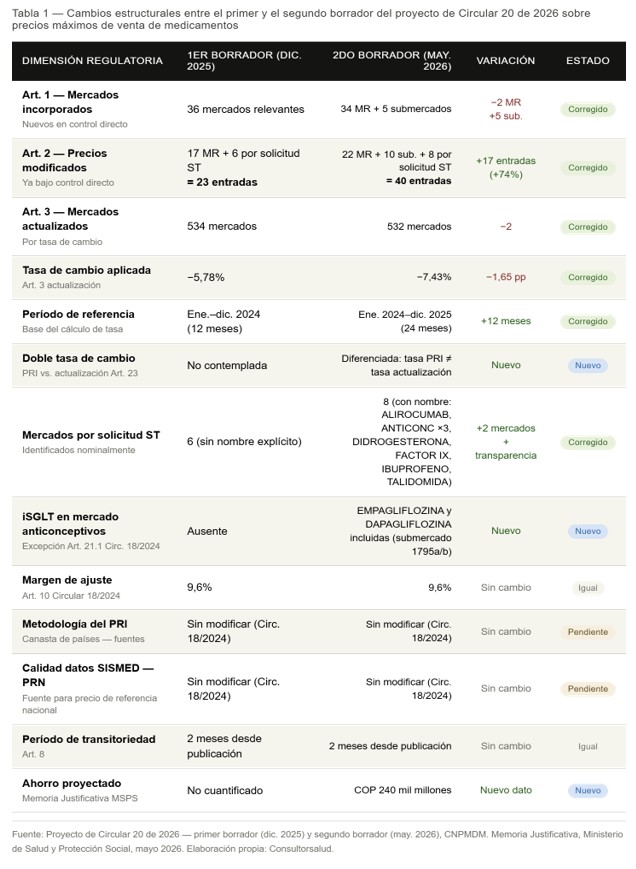
De 23 a 40 modificaciones de precio: la reconfiguración del artículo 2
El artículo 1 del segundo borrador propone incorporar al régimen de control directo de precios 34 mercados relevantes y 5 submercados. La primera versión incorporaba 36 mercados sin desglose en submercados. La reducción neta de dos mercados en el agregado refleja un movimiento interno: al menos dos mercados clasificados como incorporaciones nuevas en diciembre de 2025 aparecen en mayo de 2026 como modificaciones de mercados existentes.
El artículo 2 recoge ese desplazamiento y lo amplía. La primera versión listaba 17 mercados con modificación más 6 revisados por solicitud a la Secretaría Técnica de la Comisión —23 entradas totales—. El segundo borrador propone modificar 22 mercados relevantes y 10 submercados, más 8 mercados revisados por solicitud. Total: 40 entradas, un incremento del 74% sobre la primera versión.
Los 8 mercados revisados por solicitud están ahora identificados nominalmente —en diciembre de 2025 no lo estaban—: ALIROCUMAB – Líquido/Sólido – Inyectable, ANTICONCEPTIVO – Líquido/Sólido – Inyectable, ANTICONCEPTIVO – Sólido – Oral, ANTICONCEPTIVO – Líquido/Sólido – Intrauterino (Implante), DIDROGESTERONA – Sólido – Oral, FACTOR IX – Líquido/Sólido – Inyectable, IBUPROFENO – Líquido/Sólido – Inyectable y TALIDOMIDA – Sólido – Oral.
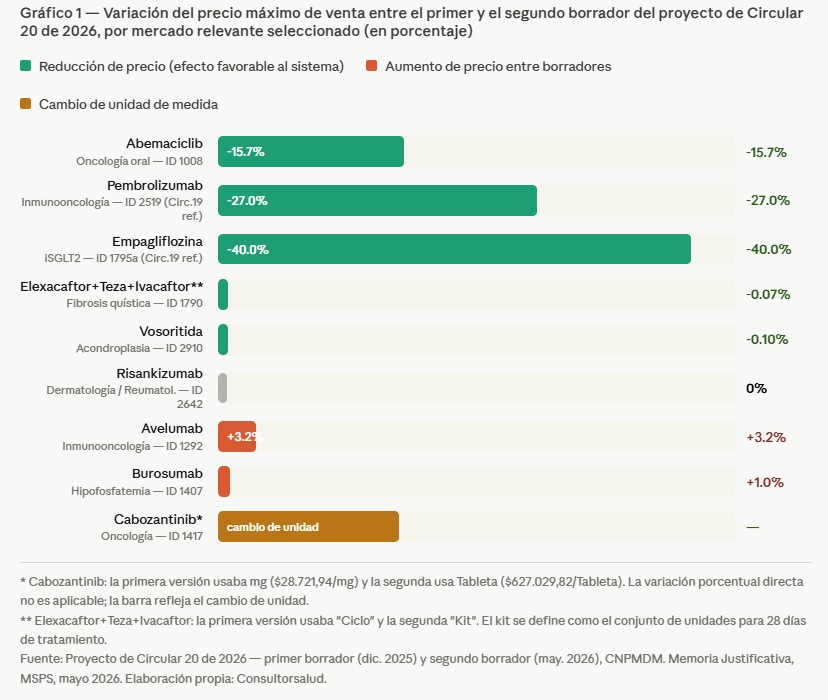
Los precios que más se mueven y por qué
La Memoria Justificativa del proyecto, publicada por el Ministerio de Salud y Protección Social en mayo de 2026, proyecta un ahorro de COP 240 mil millones en transacciones institucionales y comerciales como resultado de la aplicación de la metodología de la Circular 18 de 2024. El documento señala reducciones entre el 5% y el 93% respecto al precio de referencia nacional o al precio máximo de venta anterior, según el mercado.
ELEXACAFTOR+TEZACAFTOR+IVACAFTOR, combinación de uso específico en fibrosis quística, pasa de un precio de referencia nacional de COP $106.445.775 a un precio máximo de venta de $68.416.128,85 por kit en el segundo borrador —una reducción del 36%—. La unidad de medida cambió entre versiones: de “ciclo” a “kit”. El segundo borrador define el kit como el conjunto de unidades farmacéuticas de la combinación fija para 28 días de tratamiento, definición más precisa para la cadena de dispensación y los contratos de suministro.
PEMBROLIZUMAB y EMPAGLIFLOZINA registran reducciones del 27% y el 40% respectivamente frente a los precios de la Circular 19 de 2024, según la Memoria Justificativa. Ambos medicamentos figuran entre los de mayor valor de gasto en el sistema: PEMBROLIZUMAB por sus indicaciones en inmunooncología de amplio espectro y EMPAGLIFLOZINA por el crecimiento sostenido de su prescripción en diabetes e insuficiencia cardíaca.
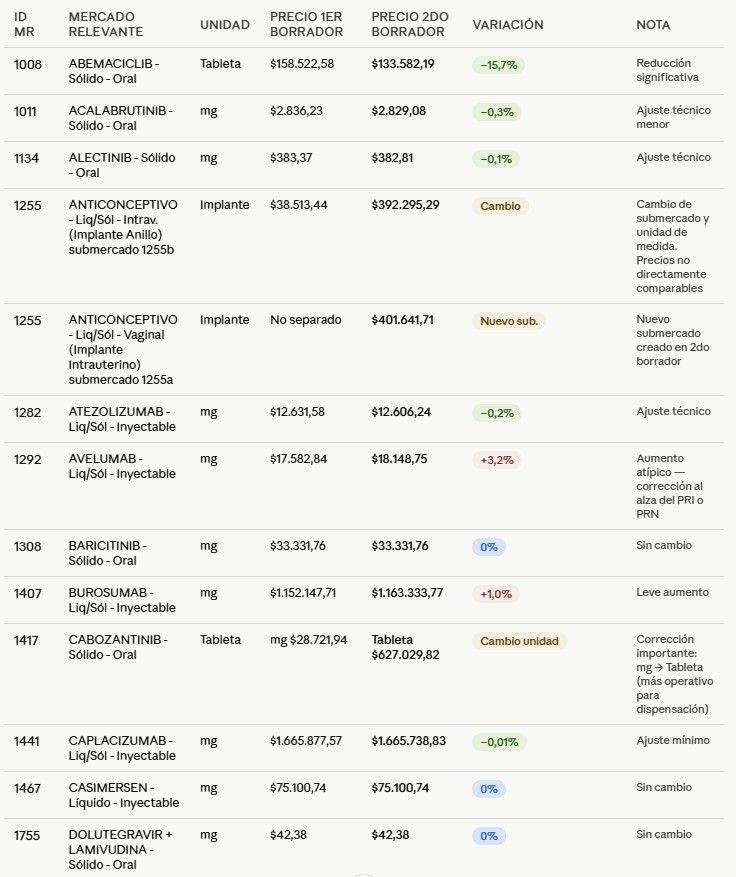
CABOZANTINIB modifica su unidad de medida entre borradores: de mg ($28.721,94/mg) a Tableta ($627.029,82/Tableta). Las presentaciones comerciales de cabozantinib disponibles incluyen tabletas de 20 mg, 40 mg, 60 mg y 80 mg. La conversión sin especificar la concentración de referencia implica que distribuidores, EPS y operadores logísticos deberán establecer contra cuál concentración se calculó ese valor para aplicarlo correctamente por presentación comercial.
El segundo borrador incorpora además el submercado 1799b: EMTRICITABINA + TENOFOVIR ALAFENAMIDA – Sólido – Oral, con precio de $61,06/mg de emtricitabina. La diferenciación entre la formulación con tenofovir disoproxil fumarato (TDF) y la formulación con tenofovir alafenamida (TAF) no existía en la primera versión, y tiene consecuencias sobre la dispensación en programas de tratamiento antirretroviral donde los dos esquemas coexisten en la misma población.
Lo que esta segunda versión no modifica porque no puede
El segundo borrador del proyecto de Circular 20 corrige el error de período en la tasa de cambio, amplía la transparencia sobre los mercados revisados por solicitud y ajusta la conformación de varios mercados relevantes. Hay materias que el texto no modifica porque están consagradas en la metodología de la Circular 18 de 2024, y una circular de aplicación no puede contradecir la circular metodológica que la sustenta.
La canasta de países de referencia para el cálculo del Precio de Referencia Internacional (PRI) y las fuentes de precio utilizadas por país fueron los temas más frecuentes en los comentarios de la primera ronda. El PRI es la mediana del precio en los países de referencia convertido a pesos colombianos usando la tasa de cambio del artículo 5 de la Circular 18 de 2024. Modificar la composición de esa canasta o las fuentes de precio requiere un proceso separado sobre la Circular 18.
La base de datos SISMED como fuente para el Precio de Referencia Nacional tampoco cambia entre borradores. Actores de la primera ronda documentaron que SISMED contiene transacciones con errores de reporte y valores atípicos no depurados, y que el estadístico del percentil 50 puede resultar en un PRN superior al precio real de negociación entre aseguradores y operadores logísticos. El diseño metodológico del PRN es, igualmente, materia de la Circular 18 de 2024.
Lo que el sector debe monitorear antes de la expedición definitiva
La segunda consulta pública del proyecto de Circular 20 está activa con un formulario articulado artículo por artículo. El período de transitoriedad propuesto es de dos meses desde la publicación en el Diario Oficial, plazo en el que los precios de la Circular 19 de 2024 mantienen vigencia para los mercados que esta circular actualiza.
El texto del segundo borrador no resuelve una pregunta operativa específica: qué tratamiento reciben los mercados relevantes incluidos en circulares anteriores a la Circular 19 de 2024 que no son objeto de actualización explícita en el artículo 3. El artículo 27 de la Circular 18 de 2024 establece que esas circulares mantienen vigencia “hasta cuando sean actualizados conforme al artículo 23”, pero el alcance de esa actualización por ciclos no queda operativizado en el proyecto. Para distribuidores y operadores logísticos que gestionan contratos de suministro con precios anclados a circulares anteriores, esa indefinición tiene consecuencias sobre la validez de los precios base en las próximas negociaciones.
La primera ronda de consulta pública sobre la regulación de precios de medicamentos demostró que los comentarios técnicos inciden sobre el contenido final del texto. Los actores que participen en esta segunda ronda disponen de la misma oportunidad antes de que la CNPMDM convoque la sesión asincrónica para la aprobación definitiva.
Fecha y hora de finalización de la publicación de este segundo borrador de regulacion de precios de medicamentos: Jueves 14 de mayo de 2026, (5:00 p.m.)
Si quiere hacer observaciones a este proyecto de circular entre aquí
Descargue el nuevo proyecto de regulacion de precios de medicamentos circular 20 de 2026 a continuación:



















