En los últimos años, la evolución en cáncer de pulmón ha sido sorprendente. En la década de los 90 a los pacientes se clasificaba por patologías en: células pequeñas o de no células pequeñas; entre el 2010 y 2013 fueron apareciendo diferentes alteraciones moleculares, primero el GFR y ALK. En los últimos siete años se ha tenido un conocimiento bastante amplio de cerca de 10 alteraciones moleculares, muchas de estas con información que permite una alta efectividad de los tratamientos.
Durante el 7mo Simposio de actualización en cáncer de pulmón convocado por la Asociación Colombiana de Hematología y Oncología – ACHO, realizado el pasado 25 y 26 de agosto, en Bogotá, el Dr. Diego Enrico, Médico Oncólogo, presentó los hallazgos y avances de la alteración de KRAS.
Mutación de KRAS e implicaciones en patologías oncológicas de pulmón
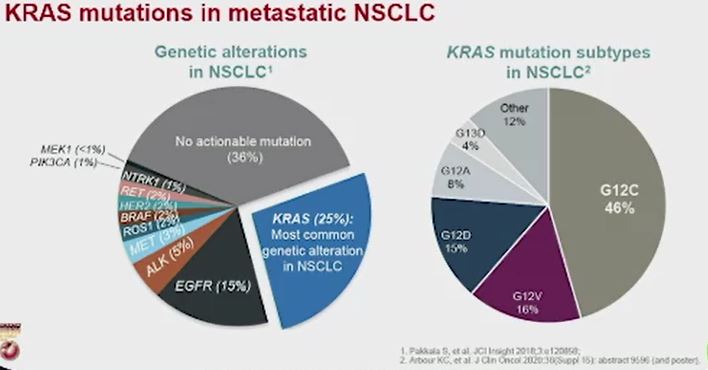
La alteración de KRAS es la más recurrente en el cáncer de pulmón, cerca del 25 al 30% de los pacientes de cáncer de pulmón células no pequeñas, pueden tener estas alteraciones, siendo la G12C la más frecuente, con un 46% y representa el 13% de los pacientes, sobre todo en pacientes con adenocarcinoma. Esta frecuencia varia depende del país, en Colombia se presenta la alteración G12C es de cerca del 8%.
KRAS es una proteína GTPase. En una célula normal, esta proteína se mantiene inactiva cuando está unida a GDP y cuando se une a GTP y se activa, provocando la cascada de señalización intracelular, el aumento de la proliferación, la supervivencia, entre otras cosas. Como explicó el Dr. Enrico, cuando se produce la mutación de G12C (sustitución de la glicina por cisteína), la proteína KRAS se activa, fomentando la proliferación y supervivencia de las células malignas. Se puede interpretar entonces al KRAS como un botón de encendido y apagado, OFF cuando está unida a GDP y ON unida a GTP.
Los pacientes con este tipo de enfermedad tienen características muy diferentes a lo que se está acostumbrado a ver. Los casos más frecuentes son en hombres, en fumadores activos o exfumadores, personas no asiáticas o suelen tener alteraciones mas altas de TMB 9.0.
Hoy en día, la detección de las anomalías o mutaciones de KRAS se hacen a través de PCR o técnicas de nueva generación (NGS), que permiten testear las 10 alteraciones moleculares del cáncer de pulmón. Aunque en los países hasta ahora se está implementando, las ventajas que brinda esta tecnología deberían incentivar su uso.
También es importante mencionar que, aunque la mutación de KRAS es muy común, los especialistas aún tienen dificultades para targetearla. Este fenómeno obedece a la alta concentración GTP y a la alta sensibilidad, lo que desencadena su fácil activación pero dificulta la posibilidad de encontrar un inhibidor eficaz.
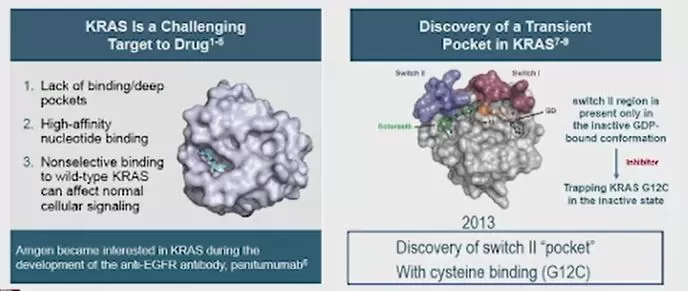
Inhibidores de KRAS
En ese camino, encontraron el lugar específico donde se puede actuar para logar frenar la activación del GTP, que funciona como un segundo bolsillo que es potencialmente accionable con un fármaco para inhibir su activación. Según el experto, esta alteración tiene alrededor de 40 años, y hasta 2013 se conoció esta posibilidad para controlarlo y hasta el 2019 llegaron estos inhibidores a las clínicas.
Aunque hay varios inhibidores en desarrollo, sin embargo, dos de los más avanzados con ensayos clínicos fase dos y tres son: el Sotorasab y el Adagrasib. El mecanismo de acción de estas moléculas es similar es una unión covalente e irreversible, que logra que la proteína se mantenga en estado inactivo, atrapándola y manteniéndola estable.
Hallazgos de Codebreak 100 y Codebreak 200
Uno de los ensayos clínicos de estos inhibidores es el CodeBreak 100, un ensayo clínico fase 2 que evalúo Sorotrasib 960 ml en una población típica de pacientes de cáncer de pulmón con alteración de KRAS, que ya habían sido expuestos a otros tratamientos, también incluía pacientes con metastasis cerebrales inactivas.
Los tratamientos que habían recibido los pacientes eran de primera, segunda y tercera línea. La mayoría, entre el 85 y 90% , habían sido tratados con quimioterapia, con la combinación quimio-inmunoterapia, o con solo inmunoterapia. La respuesta de este estudio logró una tasa de respuesta del 37%, una mediana de PFS de 6,8 meses y una tasa mediana de supervivencia global de 12,5 meses. Datos que permitieron llegar a la fase tres de este estudio.
El estudio CodeBreak 200 un ensayo clínico fase 3, como es costumbre, se testea el sotorasib versus otros tratamientos. Entre el 4 de junio de 2020 y el 26 de abril de 2021, 345 pacientes fueron asignados aleatoriamente para recibir sotorasib (n=171 [50%]) o docetaxel (n=174 [50%]). 169 (99%) pacientes del grupo de sotorasib y 151 (87%) del grupo de docetaxel recibieron al menos una dosis.
Después de una mediana de seguimiento de 17,7 meses (RIC 16,4–20,1), el estudio alcanzó su criterio de valoración principal de un aumento estadísticamente significativo en la supervivencia libre de progresión para sotorasib, en comparación con docetaxel (mediana libre de progresión). supervivencia 5,6 meses [IC 95% 4,3–7,8] vs 4,5 meses [3,0–5,7]; índice de riesgo 0,66 [0,51–0,86]; p=0 ·0017).
Sotorasib fue bien tolerado, con menos grado 3 o peor (n=56 [33%] vs.n=61 [40%]) y eventos adversos graves relacionados con el tratamiento en comparación con docetaxel (n=18 [11%] vs n=34 [23%]). Para sotorasib, los eventos adversos de grado 3 o peor relacionados con el tratamiento más comunes fueron diarrea (n = 20 [12 %]), aumento de la alanina aminotransferasa (n = 13 [8 %]) y aumento de la aspartato aminotransferasa (n = 9 [ 5%]). Para docetaxel, los eventos adversos relacionados con el tratamiento más comunes de grado 3 o peor fueron neutropenia (n=13 [9%]), fatiga (n=9 [6%]) y neutropenia febril (n=8 [5%] ).
Sotorasib aumentó significativamente la supervivencia libre de progresión y tuvo un perfil de seguridad más favorable, en comparación con docetaxel, en pacientes con NSCLC avanzado con la mutación KRAS G12C y que habían sido tratados previamente con otros medicamentos contra el cáncer.
“La medicación no solo sirve para metástasis sistémicas sino también para metástasis en el sistema nervioso central” afirmó el Dr. Enrico al cierre de su intervención en el evento organizado por la ACHO. Este estudio le dio la aprobación por la FDA en el 2021 y por la EMA en el 2022.



















