El Instituto Nacional de Vigilancia de Medicamentos y Alimentos, INVIMA, aprobó a alectinib (Alecensa®, ROCHE) para el tratamiento de carcinoma de pulmón de células no pequeñas (NSCLC por sus siglas en inglés) metastásico con mutación del ALK (ALK-positivo).
¿Qué es el alectinib?
Alectinib es un inhibidor de segunda generación, muy selectivo y potente, de la tirosina quinasa ALK y RET. En estudios preclínicos, la inhibición de la actividad de la tirosina quinasa ALK produjo un bloqueo de las vías de señalización, incluidas STAT 3 y PI3K/AKT, y la inducción de la muerte de células tumorales (apoptosis). Alectinib demostró actividad in vitro e in vivo contra las formas mutadas de la enzima ALK, incluidas las mutaciones responsables de resistencia a crizotinib. Según los datos preclínicos, alectinib no es un sustrato de la glicoproteína-P ni de la BCRP, que se consideran transportadores de membrana en la barrera hematoencefálica y, por tanto, se puede distribuir y retener dentro del SNC.
¿Qué es la ALK?
La quinasa de linfoma anaplásico (ALK, por sus siglas en inglés) es un receptor de membrana de la superfamilia de los receptores de insulina que está codificada en humanos en el cromosoma 2. La importancia de la ALK radica en que fue vinculada inicialmente con una variedad especial de linfoma (cáncer linfático), y también se asocia a el 3-5% de los NSCLC, particularmente los adenocarcinomas.
Es así que la fusión de ALK con otro gen, el EML4, es la anormalidad más frecuente en NSCLC, y causa la activación continua de la actividad tirosina quinasa de la ALK, propiciando el crecimiento y proliferación celular; la inhibición de la muerte celular programada; así como la formación de metástasis. Por esto, la fusión ALK/EML4 es considerada una mutación conductora, y se ha visto control de la enfermedad neoplásica por la inhibición de la quinasa ALK por agentes como el crizotinib y alectinib.
Evidencia clínica de alectinib en NSCLC ALK-positivo
Alectinib obtuvo aprobación regulatoria en otros países por los resultados de dos ensayos clínicos con un solo brazo de pacientes con NSLC ALK-metastásico cuya enfermedad ya no se controlaba con el tratamiento con crizotinib (Xalcori®, Pfizer, otro agente anti ALK de primera generación disponible en Colombia).
En el estudio inicial, los participantes del estudio recibieron alectinib dos veces al día para medir el efecto del medicamento. Y se observó que el 38% de los participantes experimentaron una reducción parcial de sus tumores de NSCLC, un efecto que duró un promedio de 7,5 meses. En el segundo estudio, el 44% de los participantes experimentó una reducción parcial de sus tumores de NSCLC, con una duración promedio de 11,2 meses.
Además, los ensayos también examinaron el efecto de alectinib sobre las metástasis cerebrales, una ocurrencia común en esta población. Entre los participantes en los dos ensayos, que tenían metástasis cerebrales medibles, el 61% experimentó una reducción total o parcial en sus metástasis cerebrales, con una duración promedio de 9.1 meses.
Alectinib superior a crizotinib en primera línea de NSCLC ALK-positivo
Los estudios anteriores dieron el ímpetu para la realización del estudio ALEX, un ensayo aleatorizado, multicéntrico, abierto, controlado y activo realizado en 303 pacientes con NSCLC ALK-positivo que no habían recibido terapia sistémica previa para la enfermedad metastásica. Se incluyeron pacientes tuvieran evidencia de reordenamiento de ALK. Los pacientes fueron aleatorizados 1: 1 para recibir alectinib 600 mg por vía oral dos veces al día (n = 152) o crizotinib 250 mg por vía oral dos veces al día (n = 151).
ALEX demostró una mejora en la supervivencia libre de progresión (SLP), con una razón de riesgo (HR) de 0.53. La mediana de la SLP estimada para pacientes asignados al azar a alectinib fue de 25.7 meses en comparación con 10.4 meses para aquellos asignados al azar a crizotinib. De resaltar, el tiempo para inicido de progresión específica del sistema nervioso central (SNC) también mejoró significativamente; hubo una menor incidencia de progresión en el SNC como primer sitio de progresión de la enfermedad, solo o concurrente con progresión sistémica, en el brazo de alectinib (12%) en comparación con el brazo de crizotinib (45%). La tasa objetiva de respuesta confirmada fue del 79% y 72% en los brazos alectinib y crizotinib, respectivamente. Entre los 120 respondedores en el brazo de alectinib y los 109 respondedores en el brazo de crizotinib, la proporción de pacientes con una duración de respuesta de ≥12 meses fue del 64% y 36%, respectivamente.
Es importante puntualizar que el compromiso en el SNC se evaluó en todos los pacientes. Entre los 43 pacientes con lesiones medibles del SNC en los escáneres cerebrales basales, la tasa de respuesta objetiva del SNC, fue del 81% en el brazo de alectinib y del 50% en el brazo de crizotinib.
Efectos secundarios más comunes de alectinib
Las reacciones adversas más comunes (que ocurren en ≥20% de los pacientes que toman alectinib en ALEX) fueron fatiga, estreñimiento, edema, mialgia y anemia. Se produjeron reacciones adversas graves en el 28% de los pacientes tratados con alectinib. Las reacciones adversas que condujeron a la interrupción de alectinib ocurrieron en el 11%. Las reacciones adversas que llevaron a la interrupción de alectinib en 1% o más de los pacientes fueron insuficiencia renal, hiperbilirrubinemia, aumento de alanina aminotransferasa y aumento de aspartato aminotransferasa. La interrupción de la dosis debido a reacciones adversas ocurrió en el 19% de los pacientes tratados con alectinib, mientras que se requirieron reducciones de dosis en el 16%.
Registro sanitario de alectinib en Colombia
El registro INVIMA para alectinib establece que “Alecensa está indicado para el tratamiento de pacientes con cáncer pulmonar no microcítico (NSCLC), positivo para la cinasa del linfoma anaplásico (ALK-positivo) y localmente avanzado o metastásico.”
También puede leer: 10% de los colombianos sufren de asma
Para tener en cuenta al formular alectinib
El alectinib viene en cápsulas duras de 150 miligramos. La dosis recomendada de inicio es 600 miligramos vía oral cada 12 horas. Se recomienda tomarla con alimento.
Pauta de reducción de dosis
Dosis inicial: 600 mg PO dos veces por día (BID)
Primera reducción de dosis: 450 mg PO BID
Segunda reducción de dosis: 300 mg PO BID
Suspenda si los pacientes no pueden tolerar 300 mg PO BID
Nefrotoxicidad
Grado 3: suspender temporalmente hasta que la creatinina sérica se recupere a ≤1.5x del valor superior de lo normal (ULN, por sus siglas en inglés), luego reanudar a dosis reducida.
Grado 4: descontinuar permanentemente.
Hepatotoxicidad
Elevación de ALT o AST> 5x ULN con bilirrubina total (TB, por sus siglas en inglés) ≤2x ULN: interrumpir temporalmente hasta la recuperación al valor inicial o ≤3 veces el ULN, luego reanudar a dosis reducida.
Elevación ALT o AST> 3x ULN con elevación de TB> 2x ULN en ausencia de colestasis o hemólisis: descontinuar permanentemente
Elevación de TB> 3x ULN: interrumpir temporalmente hasta la recuperación al valor inicial o ≤1.5x ULN, luego reanudar a dosis reducida
Enfermedad pulmonar intersticial (ILD, por sus siglas en inglés) / neumonitis
Cualquier grado de ILD / neumonitis relacionada con el tratamiento: suspender permanentemente
Bradicardia
Bradicardia sintomática
Suspender hasta la recuperación a bradicardia asintomática o a una frecuencia cardíaca ≥60 lpm.
Si se identifica y se suspende la medicación concomitante que contribuye, o si se ajusta su dosis, reanude alectinib a la dosis previa tras la recuperación a bradicardia asintomática o a una frecuencia cardíaca ≥60 lpm.
Si no se identifica ningún medicamento concomitante contribuyente, o si los medicamentos concomitantes contribuyentes no se suspenden o no se modifican la dosis, reanudar alectinib a dosis reducida tras la recuperación a bradicardia asintomática o a una frecuencia cardíaca ≥60 lpm.
Bradicardia potencialmente mortal o intervención urgente indicada
Suspender permanentemente si no se identifica ningún medicamento concomitante contribuyente.
Si se identifica y se suspende la medicación concomitante contribuyente, o si se ajusta su dosis, reanude alectinib a dosis reducida tras la recuperación a bradicardia asintomática o a una frecuencia cardíaca ≥60 lpm, con monitorización frecuente según esté clínicamente indicado.
Suspender permanentemente en caso de recurrencia.
CPK elevada
CPK> 5x ULN: suspender temporalmente hasta la recuperación a la línea base o ≤2.5x ULN, luego reanudar a la misma dosis.
CPK> 10x ULN o segunda aparición de> 5x ULN: suspender temporalmente hasta la recuperación al valor inicial o ≤2.5x ULN, luego reanudar a dosis reducida.
Insuficiencia renal
Leve a moderada: no se requiere ajuste de dosis.
Grave (CrCl <30 ml / min) o ESRD: no estudiada.
Alteración de enzimas hepáticas
Leve (TB ≤ULN y AST> ULN o TB> 1-1.5x ULN y cualquier AST): no se requiere ajuste de dosis.
Moderada a severa: no estudiada.
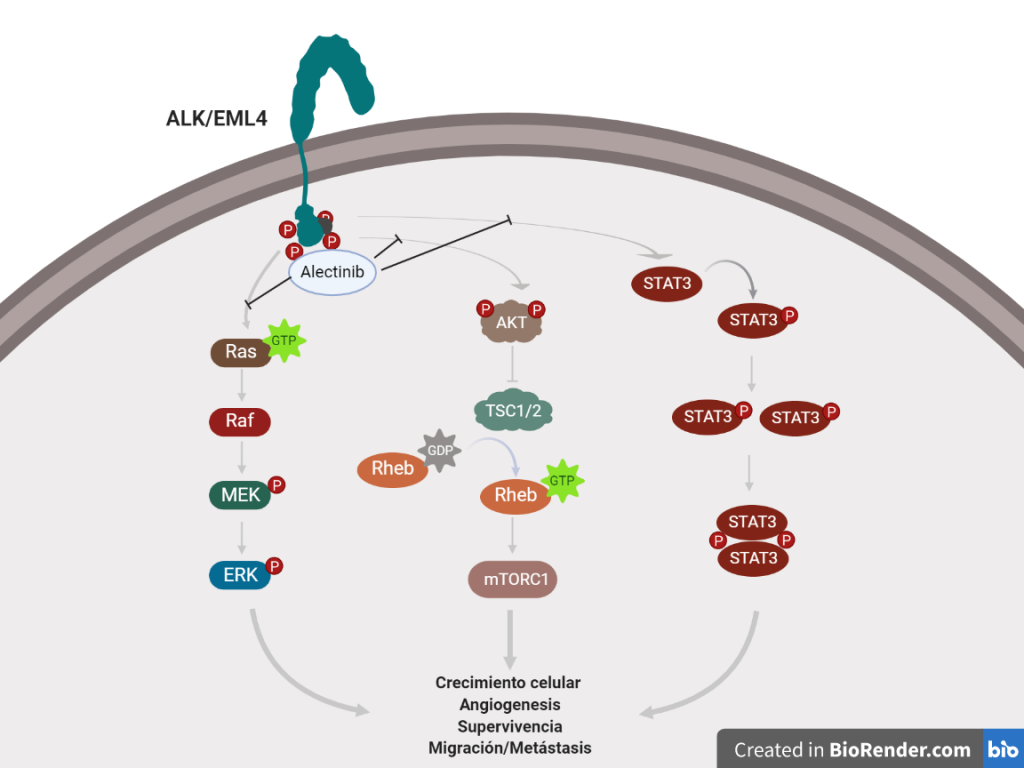
Mecanismo de acción de alectinib.
-
Oferta Producto en oferta
 XXI Congreso Nacional de SaludDesde:
XXI Congreso Nacional de SaludDesde:$2.227.680$1.713.600 (IVA incluido) -
 Muestra Comercial – XXI Congreso Nacional de SaludDesde: $6.366.500 (IVA incluido)
Muestra Comercial – XXI Congreso Nacional de SaludDesde: $6.366.500 (IVA incluido)






















