El Ministerio de Salud ha puesto a disposición del público la Circular Externa 15 de 2023. En el documento, fechado el 28 de julio, establece las disposiciones para el seguimiento del comportamiento de mercado de dispositivos médicos, el manejo del régimen de libertad vigilada. Además, se modifica la estructura del reporte de información de precios de dispositivos médicos.
La Circular 15 de 2023 es una actualización necesaria a lo estipulado en la Circular Externa 14 de 2022. Por aquel entonces, se integraron los implantes auditivos de conducción ósea, dispositivos de implante para córnea, implantables para terapia cardíaca de alto voltaje así como los implantes para implante coclear en el régimen de libertad vigilada. También se reestructuró el Sistema de Reporte de Información de Precios de Dispositivos Médicos -SISDIS-.
En consecuencia con las modificaciones, se requieren ajustes al alcance de los reportes de información de precios en la cadena de comercialización, desde los actores involucrados hasta los periodos establecidos para la entrega del reporte. “Los temas que se van a regular a través del presente acto no limitan el número o la variedad de las empresas en el mercado, ni la capacidad de éstas para competir, razón por la cual no se hace necesario solicitar concepto de abogacía de la competencia ante la Superintendencia de Industria y Comercio”, se lee en el informe.
Disposiciones generales de la Circular 15 de 2023 sobre el mercado de dispositivos médicos
Las disposiciones de la Circular 15 de 2023 serán de cumplimiento obligatorio para los actores que participan en la cadena de comercialización de los dispositivos médicos objeto de regulación de precios, realizando transacciones primarias, secundarias o finales, incluyendo los titulares de registro sanitario y a los prestadores de servicios de salud en todos los regímenes incluyendo el Especial y de Excepción.
Las autoridades en salud comenzarán con la inclusión gradual de dispositivos médicos al régimen de libertad vigilada. No obstante, y durante la implementación de este régimen, así como para la aplicación del régimen de control directo o de libertad regulada, utilizará las fuentes de información disponibles. Sobre esto último, se preferirán los datos registrados en fuentes públicas, siempre y cuando no se consideren como confidenciales según la normatividad vigente.
El periodo de referencia será entre el 1° de enero y el 31 de diciembre del año inmediatamente anterior al de la expedición de la norma que regule los precios. No obstante, si se considera pertinente, se hará una revisión y análisis del comportamiento de los precios, así como de los recobros de las tecnologías en mención. De esta manera, podrán detectarse nuevos mercados sujetos a la regulación de precios.
¿Cómo se elegirán los productos relevantes para la regulación de precios?
De acuerdo con la Circular 15 de 2023, para el control de precios se considerarán como un grupo de productos significativos aquellos que puedan ser sustituidos de manera terapéutica y/o funcional. La elección se hará teniendo en cuenta los siguientes criterios:
- Agrupaciones realizadas por nomencladores internacionales de dispositivos médicos o el estándar semántico adoptado por Colombia para dispositivos médicos de uso humano, cuando se haya establecido.
- En caso de requerirse, se complementará la información con la revisión documental de las guías, manuales y recomendaciones de uso dadas por el fabricante del dispositivo médico.
- Cuando se considere necesario, la Secretaría Técnica de la Comisión determinará las asociaciones profesionales y otros expertos del sector de los dispositivos médicos que se estén definiendo y realizará las acciones para consultar sus recomendaciones sobre el conjunto de productos relevantes, en cuyo caso las respuestas harán parte de las actas que evidencien las recomendaciones.
Los dispositivos médicos anticonceptivos que cuenten con registro sanitario ante el INVIMA, comercializados en el territorio nacional seguirán en el régimen de libertad vigilada. Esto no aplica para los dispositivos anticonceptivos usados en las IPS para exámenes diagnósticos. En el caso de los dispositivos médicos específicos bajo el régimen de libertad vigilada, se deberá seguir el procedimiento de reporte establecido que encontrará en el documento adjunto a este artículo.
Implementación del SISDIS: ¿en qué consiste?
El SISDIS es el grupo de elementos interconectados que colaboran de manera conjunta para recopilar, procesar, almacenar y divulgar información relacionada con los precios de dispositivos médicos, los cuales están contemplados en los regímenes de libertad vigilada, libertad regulada o control directo y se encuentran disponibles en el territorio nacional. El informe en SISDIS se lleva a cabo mediante la Plataforma de Intercambio de Información (PISIS) del Sistema Integral de Información de la Protección Social (SISPRO).
Dentro de sus objetivos se encuentran proveer la información necesaria a la xx, facilitar el acceso a la información no reservada sobre precios de dispositivos médicos a los actores del Sistema General de Salud y al público en general. Otro de los propósitos es normalizar el registro, almacenamiento, flujo, transferencia y disposición de la información para la regulación del mercado de dispositivos médicos en toda la cadena de producción, importación y distribución.
¿Cómo se hace el reporte en el SISDIS?
Según la Circular 13 de 2023, los fabricantes o importadores de dispositivos médicos que posean un registro sanitario emitido por el INVIMA y que hayan sido incluidos en los regímenes de libertad vigilada, regulada o control directo, así como aquellos que comercialicen o suministren dichos dispositivos, están encargados de realizar el informe de precios correspondiente en las transacciones a través del Sistema de Información de Precios de Dispositivos Médicos (SISDIS), conforme al anexo técnico adjunto a la presente circular.
Las instituciones prestadoras de salud (IPS) deben presentar informes al SISDIS sobre todas las transacciones realizadas con dispositivos médicos sujetos a los regímenes de control directo, libertad regulada o libertad vigilada en los que exista la obligación de informar.
En el caso de farmacias, droguerías y droguerías exclusivas del canal comercial, no deberán realizar el reporte al SISDIS en ninguna transacción.
Plazos para el reporte de información
La presentación de la información deberá llevarse a cabo trimestralmente, detallando las operaciones y transacciones de cada mes dentro de los plazos máximos establecidos en el siguiente calendario:
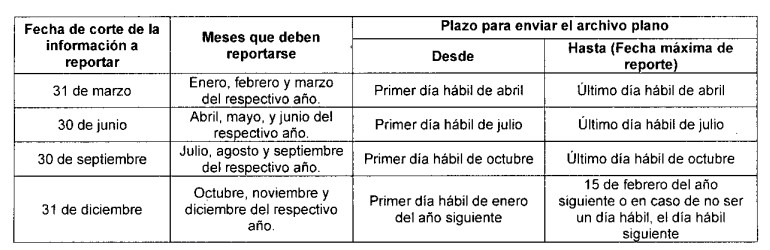
Es importante tener presente que, “la secretaría técnica de la Comisión habilitará dos veces al año el SISDIS para el reporte de casos extemporáneos así: del 1 al 21 de mayo y la segunda del 1 al 21 de noviembre, de cada vigencia; sin perjuicio de las sanciones a las que haya lugar”.



















