Cómo desearía escribir sobre cosas buenas y hermosas. Panegíricos, los llamamos. De esos que se derramaron cuando falleció un oncólogo famoso por sus contribuciones a la ciencia, que también se le olvidaba declarar sus millonarios (en dólares) ingresos por la industria farmacéutica. Ese detallito no lo mencionaron. Pero ante la tumba del Gran Hombre, es inapropiado recordar sus deslices. Todos los tenemos, los deslices. Los míos son menos lucrativos. Volveré a lo que se ha vuelto mi especialidad: la queja. En este caso, catarsis. Voy a hablar sobre lo maravilloso que es realizar investigación clínica. Doy tres casos y una conclusión.
Caso 1 – Incluir pacientes en estudios fase III es lo máximo
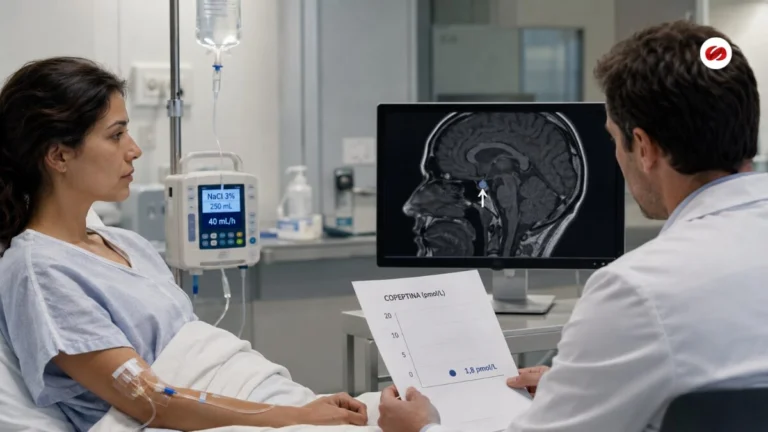
La señora tiene un cáncer avanzado, pero potencialmente curable. Es candidata para un estudio de investigación que explora la posibilidad de mejorar el control de su enfermedad a largo plazo con la adición de una nueva droga. La convencemos de que participe. Sabe que tiene que realizarse exámenes adicionales, que no requeriría en condiciones normales. Sabe también que se va a demorar en iniciar más días de lo que normalmente tendría que esperar. Pero, vale la pena ante la posibilidad de beneficiarse de la nueva droga. O, más bien, ante el 50% de probabilidad de que entre por azar al brazo de wonderlizumab (llamémosla así para no violar la confidencialidad). Cumple todos los criterios de inclusión y no sufre de ninguno de los criterios de exclusión. Vamos bien. Ya lista para la tan esperada aleatorización, cuando nos damos cuenta de que tiene un VDRL positivo. Se hace todo lo que se tiene que hacer, incluyendo punción lumbar y retratamiento con penicilina (ya había sido tratada hacía un par de años, y el episodio actual es por una CLARA reinfección).
En ese momento, el equipo técnico, detiene la aleatorización de la paciente. Estupefactos, preguntamos por qué. La respuesta: “se necesita garantizar que no tiene infección activa”. A todas estas, la resistencia a la penicilina de la sífilis es esencialmente inexistente. Los tres investigadores – todos internistas, además de oncólogos – solicitamos audiencia con el equipo técnico. Explicamos cómo no consideramos que la paciente deba ser excluida. Aducimos nuestras razones. Todo lo hacemos en nuestro inglés imperfecto. Es altamente imperfecto porque lo que nos responden en la reunión no guarda relación con lo que les planteamos.
Finalmente, nos dicen que escribamos un comunicado explicando la situación. Escribimos el comunicado lo mejor que podemos. Dos días después nos dicen que la paciente no debe ser incluida. Es importante explicar aquí que el wonderlizumab se puede dar en tuberculosos activos. Pero, según el equipo técnico gringo, no se puede dar a una sífilis latente tratada. La tragedia fue tener que explicarle a la paciente que había hecho todo su proceso con la mejor diligencia que no iba a ingresar al estudio. Y explicarle que la razón es una en la que los investigadores del centro de investigación – nosotros – no considerábamos válida.
La paciente se sintió decepcionada, defraudada y discriminada. Las tres. Tenemos un compromiso de reclutamiento de pacientes para ese estudio que no se ha satisfecho. ¿Debemos seguir reclutando para el estudio de la innovación si la inclusión de un paciente depende de la arbitrariedad de alguno que, además, no tiene en cuenta el criterio de sus investigadores en sus centros? Me sentí como Ministro de Hacienda diseñando una reforma tributaria en un país paralizado. Nosotros perdimos horas enteras en todo este affaire para al final no poder ayudar a la paciente. Pero, el tiempo de nosotros, con todo y lo importante que es, es irrelevante ante la injusticia que se cometió con esa paciente. Le hubiera ido mejor si no se le hubiera ofrecido participar en el estudio.
También puede leer: ¿Por qué fracasan los proyectos en salud?
Caso 2 – La unión hace la fuerza
Colombia está virtualmente ausente de la investigación clínica en la oncología el mundo. El porcentaje de participación del país es mínimo. Le han puesto número, que es tan bajo que lo podemos llamar infinitesimal. Varios centros participan en el reclutamiento de pacientes para estudios fase III como los que se mencionó en el apartado anterior. Pero investigación de esa originada por el investigador en Colombia hay pocos. Y la poca que hay, es por el esfuerzo de unos pocos focos. Un puñado de investigadores en Bogotá, una Sociedad Científica, y poco más. El aporte de estas iniciativas es inmenso. Ambos tienen en común que son capitalinos en su origen. ¿Qué pasa si la iniciativa no es capitalina? Aquí les cuento la experiencia de nuestra (no capitalina) institución.
Al doctor Mauricio Luján, de Medellín, se le ocurrió la idea de hacer un estudio de evidencia de vida real en pacientes con un cáncer relativamente frecuente. Se buscó la inclusión de pacientes que habían recibido tratamiento con maravillozumab (no es ironía). Como en el caso anterior, se oculta la identidad para protegerme. Pero, en vez de realizar un estudio contando la experiencia de nuestro centro, se le ocurrió realizar un estudio multicéntrico. Es decir, invitar a MUCHOS centros para incluir la mayor cantidad de pacientes posibles tratados con el agente. Se escribe el protocolo, se genera el instrumento de recolección de datos, de somete a comité de ética, y se invita a diversos centros, y personas con amplia experticia. Se estima que se pueden reclutar unos 170 pacientes. Durante casi un año perseguimos a cada uno de los centros para ver si querían participar. Menos de la mitad de los “centros” nos respondieron.
Un “investigador”, también de provincia, nos dijo que tenía cientos (nunca más volvimos a escuchar de él). El más importante de todos los expertos en Colombia no estuvo interesado en participar. Una clínica oncológica de mi ciudad dio orden de NO participar, porque la iniciativa provenía de la nuestra. Llamo al director de la clínica en cuestión, le explico la intención de trabajar en equipo. Me dice que lo va a escalar al comité de investigación. Espero pacientemente. Nada. Ni una palabra. No nos merecimos ni el no. Solo nos ignoraron. No sientan pena por mí. Yo me repongo de estos sinsabores. La grosería solo es algo desestimulante. No era una propuesta de matrimonio, era unir nuestras experiencias para poder contar una consolidada, mejor. Para hacer una historia larga corta, luego de varios partos de mula vamos a incluir unos 60 pacientes. El esfuerzo ingente, la logística, el tiempo dedicado era para que al menos cumpliéramos la meta de reclutamiento. Pero, no. No fue así. Los pocos centros que incluyeron pacientes lo hacen porque son amigos. El ego y la abulia son nuestros enemigos.
Caso 3 – Su estudio es una M
La tercera, y última, historia tiene que ver con un estudio descriptivo que sometimos a publicación en una revista colombiana de oncología indexada, de un centro oncológico capitalino. Se trataba de la descripción de nuestra experiencia con otro cáncer avanzado. Un estudio de vida real, con todas las limitaciones de un estudio descriptivo. Después de muchísimos meses, los revisores nos indican que el estudio es perverso. Recomiendan que NO se publique. Las opiniones de dos de los revisores eran idénticas. Tan congruentes como para sospechar que se trataba de un concepto “papel carbón”. De todas maneras, nos recomendaban hacerle algunos ajustes, y someterla de nuevo. Uno sabe que eso de publicar es un ejercicio en humildad. Hicimos los ajustes que nos sugirieron. La sometimos de nuevo… varios meses después, rechazaron el artículo. De nuevo, comentarios destructivos. Es impublicable, aparentemente. Busca uno en PubMed literatura sobre ese mismo cáncer en Colombia, y no encuentra NINGUNA que tenga algo que ver con la experiencia de pacientes con la enfermedad en Colombia. Es como si se pensara: si el estudio no es perfecto, es mejor no publicarlo, así llene un vacío. Afortunadamente, fue publicado en otra parte, casi un año y medio después.
Conclusión
Agradezco al lector por acompañarme en estas más de 1300 palabras. Y llega el momento de la conclusión. Por favor, redoblantes… Después de esos tres momentos que invitan a tirar todo por la borda, recibí hoy la noticia de que un paciente, del mismo Mauricio Luján, fue aleatorizado en un estudio fase III, para recibir excelentinib, droga que promete ser un estándar de tratamiento para su enfermedad. Excelentinib tiene el mecanismo de acción correcto, llena un vacío terapéutico, y es la primera vez que se usa en Colombia. Es finalmente, una pequeña contribución para que la oncología avance, que ayuda al paciente. También pienso que mi frustración de no incluir a la paciente con el wonderlizumab es precisamente porque pienso que el wonderlizumab es realmente wonderful. El estudio M se publicó. Y al final, el estudio multicéntrico se realizó, con menos pacientes, pero se realizó. Ya estamos diseñando el siguiente. Somos masoquistas.