La agencia de noticias SINC realizó una entrevista con el microbiólogo Francisco Juan Martínez Mojica, pionero de la técnica que reinventa la genética, a través de unas tijeras llamadas CRISPR/Cas9, una llave que permite para editar de forma sencilla y accesible casi cualquier rincón del genoma.
El CRISPR/Cas9, estaba a la vuelta de la esquina, inmersa en muchas de las bacterias que nos rodean.Estas tijeras de ADN guiadas por secuencias-lazarillo prometen revitalizar la terapia génica y revolucionar los tratamientos del cáncer o el sida. Incluso podría aplicarse para manipular la información genética de embriones humanos.
Por el momento este avance científico considerado el más importante del 2015 por la ´Revista Science’ cuenta con dificultades en los protocolos de seguridad al no conocerse la verdadera precisión de la técnica, y los obstáculos éticos que hay en torno a la clonación humana o el uso de células madre.
CONSULTORSALUD reproduce parte de la entrevista con el Dr. Mojica quien recientemente “comenzó una serie de investigaciones que lo llevaron a identificar muchos otros organismos y a desentrañar su papel en la biología: son autovacunas microbianas, fragmentos de virus y otras partículas que se alojan en el genoma de las bacterias como una memoria de la infección”.
¿Cómo se encontró por primera vez con las secuencias CRISPR?
Yo estaba haciendo mi tesis en una línea de investigación sobre modificaciones genéticas que provocaba la sal en ciertas regiones del genoma de la arquea. Esto alteraba el comportamiento de las proteínas que cortan ADN. Al estudiar una de estas regiones vimos que había unas secuencias espaciadas de forma regular. No sabíamos que existieran secuencias parecidas en ningún otro organismo, ni siquiera conocíamos el artículo del grupo de Japón. Por entonces no había internet, y el acceso a la información era mucho más complicado. Inmediatamente nos dimos cuenta de que lo que habíamos visto podía ser importante.
¿Por qué pensaban que esas secuencias tenían que ser importantes?
¡Porque tenían muchísimas! Y estos microorganismos no se pueden permitir el lujo de tener ornamentos en su genoma. Todo lo que tienen está aprovechado.
Y además estaban presentes en muchos más microorganismos…
Sí, después vimos el artículo de los japoneses, que las encontraron en una bacteria intestinal. En los años siguientes se fueron publicando los genomas de más microorganismos y comprobamos que estaban presentes en muchos de ellos. En el año 2000 las definimos como una familia, y por entonces las llamamos SRSR, las siglas en inglés de “repeticiones cortas regularmente espaciadas”.
¿Cuándo descubrieron su función, que funcionaban como un sistema de defensa?
En el año 2003, en una de las secuencias vimos que había un fragmento de un fago, un virus que infecta bacterias. Entonces volví a buscar en todas las secuencias disponibles y encontré fragmentos así en muchas más.
¿Podía intuirse en aquel momento su posible aplicación como una herramienta de corta-pega genético?
No. Se sabía que funcionaban como un sistema de interferencia, pero no cómo ocurría ese mecanismo: el corte de ADN que rompe a los virus y que a su vez permite la edición del genoma. Para lo que sirvió fue para llamar la atención de la comunidad científica. Un campo que estaba muerto despertó, haciendo que muchos grupos se interesaran por él hasta llegar a comprender su mecanismo y desarrollar las aplicaciones.
¿Cuál fue el punto de inflexión para llegar a la revolución que supone CRISPR?
Para mí, fue en 2011, cuando el grupo de Virginijus Siksnys, de Lituania, demostró que podía transferirse el sistema de una bacteria a otra radicalmente diferente, y que funcionaba. Eso probaba que podía usarse porque era activo en otros huéspedes. Los microbiólogos tenemos claro que ese fue un trabajo fundamental.
Usted también es responsable del nombre CRISPR, aunque en un primer momento las llamó de forma diferente. ¿Cómo surge el nuevo término?
Sí, nosotros las habíamos llamado SRSR. Pero poco después un grupo en Holanda las definió con el acrónimo SPIDER. Entonces contactaron conmigo para ver si nos poníamos de acuerdo en un nombre común. Yo les di varias opciones, incluida la de CRISPR, que fue la que se escogió porque era la más completa: corresponde a las siglas en inglés de “repeticiones cortas agrupadas regularmente y separadas en forma de palíndromo”.
CRISPR abre la posibilidad de manipular embriones humanos, no solo con fines terapéuticos, sino también para alterar rasgos o capacidades. ¿Qué opina sobre sus repercusiones éticas?
Yo soy microbiólogo, puedo dar mi opinión pero como la puede dar cualquiera de la calle. No tengo una idea formada. Lo que tengo claro es que si se quiere aplicar en algún momento tiene que seguir habiendo investigación. Cuándo y dónde nacerá un niño CRISPR no lo sé, pero ahora lo puede hacer casi cualquiera. Para legislar sobre ello no solo tienen que estar los políticos y los científicos, sino también la propia sociedad.
¿En qué está trabajando ahora?
Yo sigo con lo mío, haciendo investigación básica, sobre todo intentando entender cómo se adquieren las secuencias, como se adquiere la inmunidad, de eso no se sabe apenas nada. Aunque parece que eso no le interesa mucho a nadie.
¿Qué tal ha vivido este reconocimiento internacional como uno de los héroes CRISPR?
Yo ni siquiera tengo móvil, me gusta trabajar tranquilo, así que lo estoy viviendo con agobio y con felicidad, con muchas emociones juntas. Pero en realidad no creo que haya hecho tanto como para merecer esto. La revolución ha sido posible por el trabajo de mucha gente, yo solo hice lo que había que hacer en su momento.
Así funcionan las Tijeras Moleculares
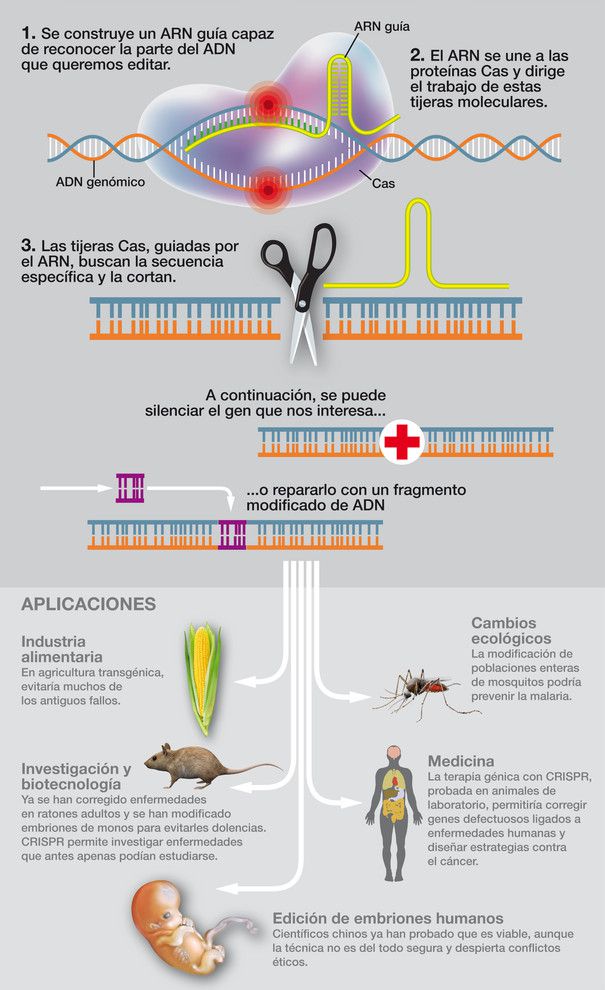
Fuente: www.agenciasinc.es





















