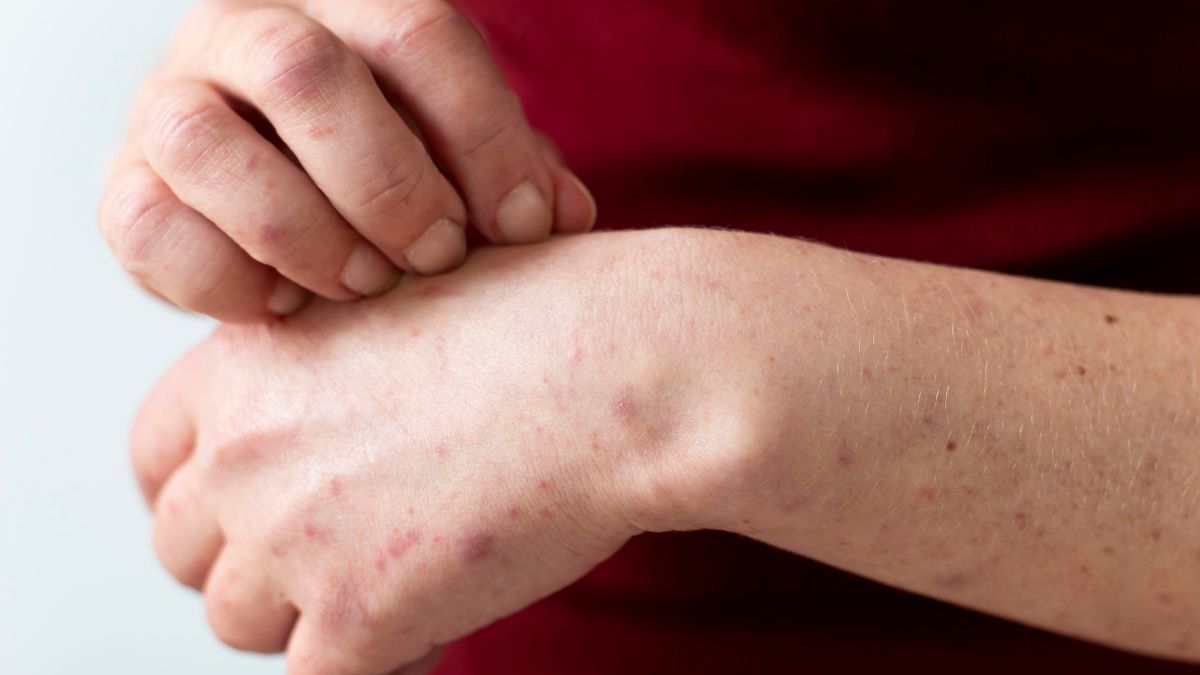
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado Ebglyss (lebrikizumab-lbkz), un medicamento desarrollado por Eli Lilly para el tratamiento de la dermatitis atópica de moderada a grave en adultos y niños mayores de 12 años. Este avance representa una alternativa crucial para aquellos pacientes cuyas condiciones no han sido controladas adecuadamente con las terapias tópicas estándar, mejorando su calidad de vida.
Ebglyss es un inhibidor de la interleucina-13, una proteína clave en el proceso inflamatorio subyacente en la dermatitis atópica. Este medicamento se administra mediante inyecciones de 250 mg/2 ml, y puede ser utilizado tanto con corticosteroides tópicos como sin ellos, brindando flexibilidad en su manejo terapéutico. La terapia comienza con una fase de inducción de 500 mg, divididos en dos inyecciones de 250 mg en las semanas 0 y 2, seguida de una dosis de mantenimiento de 250 mg cada dos semanas hasta alcanzar la semana 16 o más, momento en el cual la mayoría de los pacientes logran una respuesta clínica significativa.
Resultados prometedores de los estudios clínicos del Ebglyss
La aprobación de Ebglyss por parte de la FDA se fundamenta en los resultados de tres estudios clínicos de gran envergadura: ADvocate 1, ADvocate 2 y ADhere, en los cuales participaron más de 1.000 personas. Los estudios arrojaron resultados alentadores para los pacientes que recibieron este tratamiento. En promedio, el 38% de los pacientes tratados con Ebglyss lograron una piel limpia o casi limpia a las 16 semanas, comparado con solo el 12% de los que recibieron placebo. Además, un 10% de los pacientes experimentaron mejoras visibles tan pronto como a las 4 semanas de tratamiento.
Beneficios sostenidos en el tiempo
Una de las características más notables de Ebglyss es la durabilidad de sus efectos. Entre los pacientes que alcanzaron una piel limpia o casi limpia en la semana 16, el 77% logró mantener estos resultados durante un año completo con una dosis mensual. Incluso aquellos que cambiaron de Ebglyss a placebo después de la semana 16, mantuvieron los resultados durante un año en el 48% de los casos.
Además de mejorar el aspecto de la piel, Ebglyss también fue efectivo en reducir el picor, uno de los síntomas más debilitantes de la dermatitis atópica. El 43% de los pacientes experimentó una disminución significativa del picor a las 16 semanas, en comparación con solo el 12% en el grupo placebo, lo que demuestra un impacto importante en la mejora de la calidad de vida de los pacientes.
El desafío de la dermatitis atópica en la actualidad
El Dr. Jonathan Silverberg, MD, Ph.D., de la Universidad George Washington y primer autor de un artículo publicado en el New England Journal of Medicine, subrayó la importancia de esta nueva opción terapéutica en un comunicado de prensa. “Los pacientes aún tienen dificultades para controlar su dermatitis atópica moderada a grave con las terapias disponibles en la actualidad”, explicó el Dr. Silverberg. “Muchos experimentan un control deficiente de la enfermedad a largo plazo, y la picazón intensa puede afectar significativamente su vida diaria”.
Un paso adelante en el tratamiento de la dermatitis atópica
La aprobación de Ebglyss abre nuevas posibilidades en el manejo de la dermatitis atópica, brindando una opción más eficaz para aquellos pacientes que no responden adecuadamente a los tratamientos convencionales. A medida que más personas se beneficien de este medicamento, se espera que mejore significativamente su calidad de vida, reduciendo el impacto negativo de los síntomas sobre sus actividades diarias y bienestar emocional.
Con este importante avance, Eli Lilly reafirma su compromiso con la innovación en el campo de la dermatología, brindando a los pacientes una nueva oportunidad para vivir una vida más plena y libre de los síntomas debilitantes de la dermatitis atópica.