Si no entiendes que es el precio basado en valor para los nuevos medicamentos en colombia, si estás confundido sobre cuales son las categorías de precio basado en valor y que significa cada una, si no conoces cuales son las evaluaciones que el IETS realizará a estas moléculas, si no entendiste la circular 16 de 2023 pero estás preocupado por el futuro terapéutico y la innovación, si quieres conocer mas sobre escaneo de horizontes, los comparadores terapéuticos y la calidad de la evidencia, este artículo que revisa el manual metodológico del IETS sobre la categoría de valor terapéutico para nuevos medicamentos es para ti.
Que es el Manual metodológico para la definición de la categoría de valor terapéutico?
El manual proporciona una metodología para determinar la categoría de valor terapéutico de medicamentos, de acuerdo con el artículo 72 de la Ley 1753/2015. El objetivo es establecer una guía para la evaluación de nuevos medicamentos y su categorización basada en su valor terapéutico adicional.
Estructura general del manual metodológico para la definición de la categoría del valor terapéutico
El manual consta de cinco capítulos. El primer capítulo brinda una visión general del propósito y antecedentes del manual. El segundo capítulo detalla la metodología para determinar la categoría de valor terapéutico, incluyendo la selección y calificación de medidas de resultado, tipos aceptables de evidencia, selección de comparadores terapéuticos y evaluación de la certeza de la evidencia.
El tercer capítulo describe la metodología para llevar a cabo diálogos tempranos, que son oportunidades de intercambio de información y discusión sobre el alcance de la evaluación. Explica el proceso de exploración y presentación de formularios de solicitud de diálogos.
El cuarto capítulo proporciona una lista de referencias utilizadas en el desarrollo del manual. Por último, el quinto capítulo contiene anexos, como un formulario para solicitar los diálogos tempranos.
Capítulo 1 – Contexto y propósito
En este capítulo se establece el contexto y el propósito del manual. Se menciona que la evaluación del Instituto de Evaluación Tecnológica en Salud (IETS) de los medicamentos definidos por el Ministerio de Salud y Protección Social (MSPS) es un requisito para determinar el precio fijado por la Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos (CNPMDM). Se hace referencia a la reglamentación del artículo 72 de la Ley 1753/2015 y se menciona que este manual define la metodología para clasificar el valor terapéutico de los medicamentos nuevos.
Capítulo 2 – Metodología para determinar la categoría de los medicamentos
En este capítulo se detalla la metodología para determinar la categoría de valor terapéutico de los medicamentos. Se abordan aspectos como la selección y calificación de las medidas de resultado, los tipos de evidencia aceptables para el análisis, la elección de comparadores terapéuticos y la evaluación de la certeza de la evidencia. Se ofrecen pautas para llevar a cabo la evaluación de acuerdo con los criterios establecidos en el Decreto 433/2018.
Capítulo 3 – Metodología para llevar a cabo diálogos tempranos
Este capítulo se enfoca en la metodología para llevar a cabo diálogos tempranos, que son oportunidades de intercambio de información y discusión sobre el alcance de la evaluación. Se explica el proceso de exploración del horizonte y se proporciona un formulario para solicitar los diálogos tempranos. Se destaca la importancia de estos diálogos en la evaluación de los medicamentos y se brindan pautas sobre cómo utilizar esta estrategia de manera efectiva.
Capítulo 4: Listas de referencia
En este capítulo se presenta una lista de referencias que fueron utilizadas en el desarrollo del manual. Estas referencias son fuentes de información y evidencia científica que respaldan la metodología y los criterios establecidos en el manual.
Capítulo 5 – Anexos
El último capítulo contiene anexos que complementan la información del manual, como formularios y herramientas adicionales que pueden ser útiles para llevar a cabo la evaluación de los medicamentos y clasificar su valor terapéutico.
Términos claves del Manual metodológico para la definición de la categoría de valor terapéutico
Aproximación GRADE:
Es un sistema para calificar la calidad del cuerpo de la evidencia en revisiones sistemáticas y otras síntesis de evidencia, como evaluaciones de tecnologías en salud y en guías, y formular recomendaciones en salud. La aproximación GRADE ofrece un proceso transparente y estructurado para desarrollar y presentar los resúmenes de la evidencia, y para llevar a cabo los pasos que implica la formulación de las
recomendaciones. Se puede utilizar para desarrollar guías de práctica clínica (GPC) y otras recomendaciones del área de la salud (p.ej. salud pública, sistemas y políticas públicas y decisiones de cobertura en salud).
Asignación aleatoria:
Se refiere a un proceso predefinido (p. ej., aleatorización) especificado en un protocolo aprobado que estipula la asignación de sujetos de investigación (individualmente o en grupos) a uno o más brazos (p. ej., intervención, placebo u otro control) de un ensayo clínico (2).
Calidad de la evidencia/certeza en la evidencia:
En el contexto de una revisión sistemática, las calificaciones de la calidad de la evidencia reflejan el grado de nuestra confianza en que las estimaciones del efecto son correctas y, en el caso de las recomendaciones, las calificaciones de calidad reflejan el grado de nuestra confianza en que las estimaciones de un efecto son adecuadas para respaldar una decisión o recomendación en particular.
Comparador terapéutico:
“(…) mejor opción terapéutica, usada de manera rutinaria en nuestro país, a la luz de la mejor evidencia científica disponible y a criterio de los clínicos prescriptores, de conformidad con los manuales metodológicos establecidos por el Instituto de Evaluación Tecnológica de Salud (IETS). En el caso de medicamentos, es aquel que cuenta con registro sanitario expedido por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA), y que ha demostrado el mejor comportamiento en seguridad y eficacia o efectividad en una indicación específica”.
Desenlace crítico:
“(…) son los resultados clínicos críticos para el cuidado de la salud de los individuos y que permiten tomar decisiones frente a una opción terapéutica específica. Los desenlaces críticos para realizar la evaluación objeto del presente título serán definidos por el IETS y serán el punto de partida para desarrollar todas las etapas de la evaluación”.
Efectos dramáticos:
Efectos del tratamiento en los que los sesgos -como una posible explicación- pueden ser descartados sin experimentos clínicos aleatorizados; pueden definirse por el tamaño del tratamiento (señal) relativo al pronóstico esperado (ruido): si la razón señal/ruido es grande (por encima de 10) los efectos reales del tratamiento son probables (5). En la aproximación GRADE se considera que existe un efecto grande si el
riesgo relativo es mayor a 2 o menor a 0,5; y un efecto muy grande si el riesgo relativo es mayor a 5 o menor a 0,2; otros autores sugieren que el efecto es muy grande si el riesgo relativo es 10 o mayor (6).
Ensayo clínico aleatorio: “(…) un estudio de investigación en el que uno o más sujetos humanos se asignan prospectivamente a una o más intervenciones (que pueden incluir un placebo u otro control) para evaluar los efectos de esas intervenciones en los resultados biomédicos o conductuales relacionados con la salud”.
Escaneo de horizonte:
“(…) actividad de verificación sistemática para identificar oportunidades, problemas o amenazas relacionadas con tecnologías en salud no comercializadas, con el fin de poder obtener información que sirva para la toma de decisiones en sus usos futuros”.
Heterogeneidad clínica:
Hace referencia a la situación en la cual la asociación de intervención y desenlace es diferente de acuerdo al nivel un factor específico definible adicional, lo que también se puede interpretar como un modificador del efecto.
Intervención:
Se define como una manipulación del sujeto o del entorno del sujeto con el propósito de modificar uno o más procesos biomédicos o conductuales relacionados con la salud o criterios de valoración. Los ejemplos incluyen: fármacos/moléculas pequeñas/compuestos; biológicos; dispositivos; procedimientos (por ejemplo, técnicas quirúrgicas); sistemas de entrega (por ejemplo, telemedicina, entrevistas cara a cara); estrategias para cambiar el comportamiento relacionado con la salud (p. ej., dieta, terapia cognitiva, ejercicio, desarrollo de nuevos hábitos); estrategias de tratamiento; estrategias de prevención; y, estrategias diagnósticas. Para el proceso de definición de valor terapéutico adicional, en el manual, la intervención se refiere a los medicamentos o moléculas que se están evaluando.
Orden y tipos de desenlaces que debe ser evaluados
El manual establece el orden y los tipos de desenlaces que deben ser evaluados para determinar el valor terapéutico adicional de un medicamento. Según el Manual metodológico del IETS, la selección y gradación de desenlaces debe realizarse siguiendo ciertas indicaciones.
El orden para escoger un desenlace de eficacia o efectividad dependerá de la historia natural de la enfermedad y la dimensión que se quiera abordar. Se aceptarán desenlaces que hayan sido evaluados como el desenlace principal en al menos una investigación que respalde la solicitud del proponente.
En el proceso de evaluación, se seleccionarán los desenlaces calificados como críticos e importantes según la metodología GRADE. Los desenlaces críticos se refieren a aquellos que tienen un impacto significativo en la salud del paciente, mientras que los desenlaces importantes son aquellos que también tienen relevancia clínica, pero en menor medida.
Si la evaluación se basa en desenlaces clínicos importantes, la clasificación del valor terapéutico adicional del medicamento estará entre las categorías tres a cinco.
En el caso de enfermedades con mortalidad importante, se deben evaluar desenlaces relacionados con la mortalidad y el aumento del riesgo de mortalidad, como la muerte por cualquier causa o la probabilidad de progresión de la enfermedad hacia este desenlace.
Tipo de evidencia que se considera aceptable para el análisis
El manual tambien describe el tipo de evidencia que se considera aceptable para el análisis en la evaluación del valor terapéutico adicional de un medicamento. Según el Manual metodológico del IETS, se establecen ciertos criterios para determinar qué tipo de evidencia se puede utilizar en el proceso de evaluación.
En primera instancia, se dará preferencia a la evidencia derivada de Ensayos Clínicos Aleatorizados (ECA). Esto significa que los análisis se basarán en los resultados obtenidos de estudios científicos rigurosos en los que los participantes son asignados aleatoriamente a diferentes grupos de tratamiento.
Cuando existan múltiples ECA disponibles, se realizará un metanálisis utilizando la técnica de efectos aleatorios. Este metanálisis combinará y analizará los resultados de cada uno de los desenlaces relevantes en cuanto a efectividad y seguridad. Además, si los ECA utilizan un comparador que no es considerado la mejor alternativa disponible en Colombia, se realizarán comparaciones indirectas utilizando idealmente el metanálisis en red.
Además de los ECA, se tomará en cuenta la evidencia proporcionada por los estudios fase 4 y las alertas sanitarias publicadas por las agencias sanitarias a nivel mundial. Estos estudios y alertas proporcionan información adicional sobre la seguridad del medicamento.
En general, se aceptará como evidencia solamente los estudios que sean Ensayos Clínicos Aleatorizados, a menos que se justifique adecuadamente el uso de otra evidencia. Un ejemplo de este caso son las enfermedades ultra-raras, donde es difícil reclutar un número suficiente de participantes para realizar ECA clásicos. Sin embargo, incluso en estos casos, se exigirá que la evidencia incluya una comparación con una fuente de control apropiada.
En resumen, la evidencia considerada aceptable para el análisis en la evaluación del valor terapéutico adicional de un medicamento incluye Ensayos Clínicos Aleatorizados como primera opción. En caso de existir múltiples ECA, se realiza un metanálisis. Además, se consideran los estudios fase 4 y las alertas sanitarias. En circunstancias excepcionales, se podrán aceptar otros tipos de evidencia, pero se requiere una justificación sólida para su uso.Algoritmo de decisión utilizado para asignar la categorías
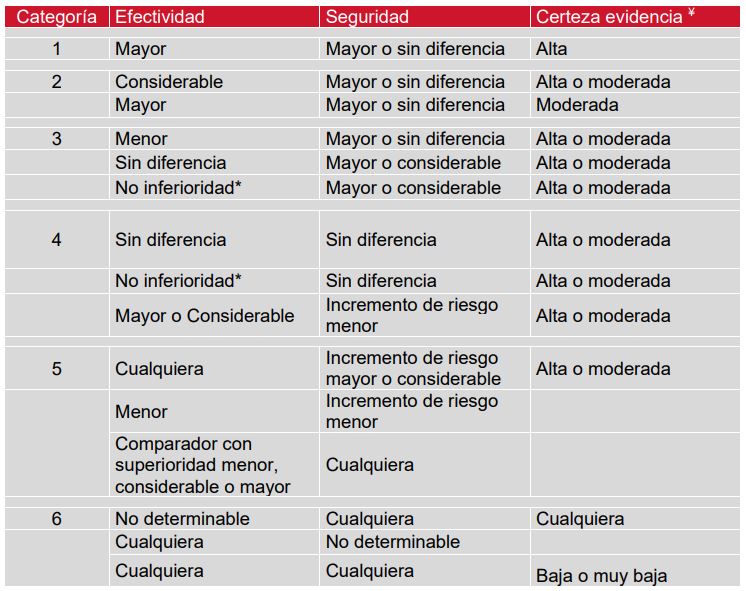
El documento describe el algoritmo de decisión utilizado para asignar las categorías de valor terapéutico a los medicamentos en el marco del artículo 72 de la Ley 1753/2015. Este algoritmo se basa en una metodología específica que se detalla en el Manual metodológico para la definición de la categoría de valor terapéutico.
El proceso de asignación de categorías de valor se realiza siguiendo una serie de pasos y consideraciones. En primer lugar, se evalúa la evidencia disponible, que incluye los desenlaces clínicos y de seguridad reportados en los estudios clínicos. Se utilizarán análisis estadísticos y criterios establecidos para evaluar la magnitud del efecto de los desenlaces ordinales y binarios.
Después de evaluar la evidencia, se procede a determinar la categoría de valor terapéutico. Este proceso se basa en un algoritmo que tiene en cuenta múltiples factores, como la eficacia, la seguridad, la relación con el comparador y el impacto en la calidad de vida del paciente.
La metodología para asignar la categoría de valor terapéutico incluye la gradación de la calidad de la evidencia, la evaluación de la magnitud del efecto terapéutico y la consideración de otros aspectos relevantes, como el costo y el contexto terapéutico.
En resumen, el algoritmo de decisión para asignar las categorías de valor terapéutico se basa en una metodología que evalúa la evidencia disponible, considerando la eficacia, seguridad y otros factores relevantes. La gradación de la calidad de la evidencia y la evaluación de la magnitud del efecto son pasos importantes en este proceso. El objetivo es determinar la categoría de valor terapéutico de un medicamento de acuerdo con criterios establecidos.
Descargue el Manual metodológico del IETS para asignar las categorías de valor terapéutico para nuevos medicamentos





















