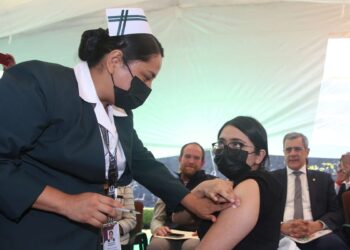
A través de un nuevo proyecto de decreto, el Ministerio de Salud ha dado a conocer ajustes a las políticas de uso de componentes anatómicos, con el propósito de optimizar su distribución para facilitar su acceso a los usuarios del sistema de salud en condiciones de calidad, oportunidad y seguridad. En este documento, la máxima autoridad sanitaria del país reconoce la importancia de la sustitución de órganos, tejidos o células; el apoyo de estos componentes en procesos biológicos y la posibilidad que éstos brindan para elaborar productos basados o derivados que se destinan a la aplicación clínica.
En el país, la Ley 1805 de 2016 ratificó la existencia de la Red de Donación y Trasplantes de Órganos y Tejidos, para garantizar la cadena de custodia durante todo el proceso de donación, así como el uso final de estos componentes anatómicos; la red está a cargo del Instituto Nacional de Salud (INS) para su estructura y organización. Además, en la misma ley, se creó el derecho a la oposición de la presunción legal de donación y a que se respete a la voluntad expresada en vida sobre el tema.
También le puede interesar: Minsalud e INS deberán modificar lineamientos para la donación de sangre: Corte Constitucional
Pese a que se trata de una herramienta fundamental dentro del sistema de salud colombiano, no todas las necesidades de la población son cubiertas. Con el paso del tiempo, ha surgido la necesidad de crear la Red de Bancos de Leche Humana y la Red de Biobancos; también se requiere implementar buenas prácticas para la donación, evaluación, obtención, preservación, almacenamiento, transporte, uso y disposición final de estos componentes anatómicos.
De acuerdo con lo anterior, el proyecto de decreto será de aplicación obligatoria para el INS, el Instituto Nacional de Vigilancia de Medicamentos y Alimentos – INVIMA, el Instituto Nacional de Medicina Legal y Ciencias Forenses -INMLCF, las Entidades Administradoras de Planes de Beneficios- EAPB, las Instituciones Prestadoras de Servicios de Salud – IPS, las Direcciones Departamentales y Distritales de Salud, los bancos de células, de tejidos, de leche humana y Biobancos.
No olvide leer: Componentes Anatómicos – Donación e Investigación – Decreto
Las disposiciones también regirán para las personas, instituciones o establecimientos dedicados a todas o algunas de las actividades relacionadas con donación, obtención, evaluación, extracción de componentes anatómicos de origen anatómicos con fines de diagnóstico, docencia, investigación, terapéuticos y preventivos, y, para las personas jurídicas sin ánimo de lucro que se dediquen a la elaboración, importación, exportación, almacenamiento y distribución de productos basados en células y tejidos humanos.
Los bancos nacionales de células y de tejidos nuevos, los bancos de tejidos que incorporen un nuevo tejido o nueva técnica de procesamiento o preservación, deberán contar con un certificado de cumplimiento de condiciones sanitarias que tendrá una vigencia de un (1) año, mientras obtienen el certificado de buenas prácticas expedido por el INVIMA.
Le puede interesar: Fernando Ruiz podría ser el próximo director de la Organización Panamericana de la Salud -OPS-
1. ¿Qué es el Sistema de Componentes Anatómicos?
De acuerdo con este proyecto de decreto, se define como Sistema de Componentes Anatómicos a la integración de las redes vinculadas con componentes anatómicos. Aquí se incluye la Red de Donación y Trasplantes de Órganos, Tejidos y Células; la Red de Bancos de Leche Humana; la Red de Biobancos y aquellas que el Ministerio de Salud disponga.
Las redes permiten optimizar la donación, el uso y distribución de los componentes anatómicos y favorecer el acceso de las personas a estas tecnologías en salud, en condiciones de calidad, oportunidad y suficiencia. Según el documento, en el país existen las siguientes:
- Red de Donación y Trasplantes de órganos, tejidos y células: compuesta diferentes instituciones (INS, INVIMA, Instituto Nacional de Medicinal Legal, EAPB, IPS habolitados para realizar trasplantes o generar donantes, entre otras) para coordinar actividades relacionadas con la promoción, notificación, donación, extracción, transporte y trasplante de células, tejidos y órganos para hacerlos accesibles en condiciones de calidad, en forma oportuna y suficiente a la población.
- Red de Biobancos: redes integradas por el INS, el INVIMA, las Direcciones Departamentales y Distritales de Salud, los Biobancos y otros integrantes del Sistema General de Seguridad Social en Salud – SGSSS para coordinar actividades relacionadas con la promoción, donación, extracción y uso de muestras biológicas, con el objeto de suministrarlas para fines de investigación.
- Red de Bancos de Leche Humana: está integrada por el INS, el INVIMA, el Instituto Colombiano de Bienestar Familiar – ICBF-, las Direcciones Departamentales y Distritales de Salud y los demás integrantes del SGSSS, para la coordinación de actividades relacionadas con la promoción, donación, extracción y uso de leche humana, con el objeto de hacerla accesible en condiciones de calidad, en forma oportuna y suficiente a la población.
Le puede interesar: Logran primer trasplante de hígado acondicionado en una máquina
El Ministerio de Salud realizará la evaluación y seguimiento a las redes de donación y trasplantes, de órganos, tejidos y células, de bancos de leche humana y de biobancos de conformidad con los lineamientos y la información que entregue la coordinación nacional de estas redes.
Cabe mencionar que, los bancos nacionales de células, de tejidos, de leche humana y los biobancos, deberán inscribirse ante la respectiva Coordinación Territorial de las Redes de Componentes Anatómicos del respectivo ente territorial. No obstante, para su funcionamiento tendrán que certificarse en buenas prácticas – BP y cumplir con las condiciones técnicas, locativas, sanitarias, higiénicas y de control de calidad establecidos en Guía de Verificación de Buenas Prácticas – BP y las modificaciones del INVIMA.
2. ¿Cuáles serán los requisitos de asignación, rescate y distribución de componentes anatómicos?
Los requisitos presentados por el Ministerio de Salud serán de obligatorio cumplimiento para las IPS habilitadas para realizar trasplantes, la Coordinación Nacional y la Coordinación Territorial. Dichas condiciones se dividen en ‘requisitos de asignación’ y ‘requisitos de rescate’ que serán descritos a continuación:
Requisitos de asignación de componentes anatómicos:
– Los componentes anatómicos serán asignados a los pacientes, de conformidad con los criterios únicos nacionales definidos por el INS para cada tipo componente anatómico, y su correspondiente actualización.
– Previo a la asignación del componente anatómico, se deben realizar estudios al potencial donante con pruebas de laboratorio especializadas requeridas para la generación del matching, por lo cual es necesario que exista de manera permanente una institución prestadora de servicio de salud – IPS de turno que asegure esta obligación. Las Coordinaciones Territoriales serán las encargadas de programar los turnos y de incluir el nivel de la IPS para el matching.
Le puede interesar: Minsalud habilitaría nueva plataforma para reporte de hechos vitales
– Cada vez que se oferte un componente anatómico, el INS generará listas ordenadas de pacientes mediante matching. Se contemplarán como categorías las siguientes: IPS, municipio, distrito o departamento cuando el donante se encuentre en un área con prestadores habilitados para realizar trasplantes. Si el donante se encuentra en un departamento sin prestadores habilitados para el procedimiento, únicamente se generará match nacional con las mismas categorías.
– La Coordinación Territorial en donde se ubiquen las instituciones prestadoras de servicios de salud que realizan procedimientos de trasplante, utilizará la lista ordenada de pacientes que generó el matching en orden ascendente por municipio o distrito y departamento, cuando el componente no ha sido aceptado en la IPS trasplantadora.
– La Coordinación Nacional ofertará los componentes anatómicos que no hayan sido aceptados a nivel departamental, utilizando el orden de la lista de pacientes que ha sido generada en el matching nacional.
No olvide leer: ¿Quiénes son los candidatos para dirigir la OPS?
Requisitos para el rescate de componentes anatómicos:
– Las IPS habilitadas para realizar trasplantes deben garantizar la disponibilidad permanente para el rescate de componentes anatómicos todos los días del año.
– Para el caso de rescate de riñón, por necesidades técnicas, se establecerán turnos por parte de la Coordinación Territorial.
– La Coordinación Territorial establecerá turnos de rescate entre los prestadores habilitados para trasplantes ubicados en su jurisdicción para la extracción y envío de componentes anatómicos entre municipios, distritos y departamentos, cuando se trate de oferta nacional.
En el documento, también se especifican los requisitos para la obtención, distribución y utilización de los componentes anatómicos. Lo anteriormente mencionado se priorizará de la siguiente manera:
- Las IPS habilitadas para realizar trasplantes, determinarán si pueden utilizar dentro de su institución, el componente anatómico que han rescatado; de ser así, deberán informar a la Coordinación Territorial. Si las IPS no pueden cumplir con los criterios de asignación definidos por el INS, deberán informar a la Coordinación Territorial sobre el no uso del componente anatómico rescatado.
- La Coordinación Territorial, una vez tenga conocimiento sobre la no utilización del componente anatómico rescatado, deberá ofertarlo entre las IPS habilitadas para realizar procedimientos de trasplantes de su municipio, distrito o departamento e informarlo a la Coordinación Nacional.
- Si en el municipio, distrito o departamento no exista receptor en la IPS habilitada, de acuerdo con los criterios de asignación del INS, la Coordinación Territorial informará a la Coordinación Nacional para que ésta proceda con la oferta nacional y asignación, en cualquiera de los otros departamentos.
Le puede interesar: Colombia, presidente de la Red Americana de Cooperación sobre Salud Electrónica – RACSEL
En cuanto a la cadena de custodia que requieren los órganos y tejidos para su conservación, cuando se trate de donantes fallecidos por muerte violenta u otras causas que requieran necropsia médico-legal, las IPS y laboratorios clínicos donde se ubique el cádaver serán responsables de la cadena de custodia de los componentes anatómicos, relacionados con la evidencia física y elementos materiales probatorios. En ese sentido, deberán responder por ellos ante la autoridad judicial competente.
Las entidades beneficiadas con el suministro de cadáveres para fines de docencia o investigación, deberán informar al Instituto Nacional de Medicina Legal y Ciencias Forenses, el sitio en donde queda dispuesto el cadáver. En el proceso, serán las entidades beneficiarias las responsables de la cadena de custodia del cuerpo y las que responderán ante la autoridad judicial competente de ser necesario.
Las instituciones de educación superior y centros científicos acatarán los principios establecidos en el Manual del Sistema de Cadena de Custodia emitido por la Fiscalía General de la Nación y los procedimientos definidos por el Instituto Nacional de Medicina Legal y Ciencias Forenses para garantizar la cadena de custodia y verificación de modificaciones introducidas en los cadáveres en cada etapa del estudio, así como la normatividad vigente para la disposición final de los mismos.
Le puede interesar: Procuraduría pide a la Supersalud intervenir Ecoopsos EPS
3. ¿Cuáles serán las responsabilidades de las EAPB en materia de trasplantes?
De acuerdo con el proyecto de decreto, cuando la IPS habilitada para realizar trasplantes determine que un paciente es apto para el procedimiento y sea ingresado a la lista de espera de donación, las EAPB deberán autorizar la realización del trasplante, la valoración previa, el seguimiento y el suministro de medicamentos, entre otros procesos relacionados de manera integral y oportuna.
Asimismo, las entidades eberán entregar los medicamentos inmediatamente después sean prescritos a los pacientes trasplantados, cuando su indicación haya sido aprobada por la autoridad competente. Si la entrega de medicamentos es incompleta, las EAPB deberán entregar los faltantes dentro de las 48 horas siguientes a la prescripción.
Las EAPB deberán reconocer a las IPS los costos asociados a la donación, trasplante o la utilización de componentes anatómicos, según los lineamientos del Ministerio de Salud. Por su parte, la Superintendencia Nacional de Salud velará por el cumplimiento de lo dispuesto en materia de trasplantes para los usuarios del sistema de salud.
No olvide leer: Nuevo plazo podría salvar las EPS del país – Proyecto de decreto
4. ¿En qué consistirá el Sistema Nacional de Biovigilancia, inspección y control sanitario de componentes anatómicos?
En el decreto en borrador, las autoridades crean el Sistema Nacional de Biovigilancia para identificar, registrar, analizar y evaluar de manera sistemática los incidentes y eventos adversos en los procesos de donación, trasplante y uso de componentes anatómicos. El Ministerio de Salud definirá os lineamientos generales para su operación, sin afectar los requisitos o lineamientos que emitan el INS, el INVIMA y las direcciones departamentales y distritales de salud.
El INVIMA, en coordinación con las direcciones departamentales o distritales de salud, ejercerá las funciones de inspección, vigilancia y control sanitario a los bancos de células, tejidos, leche humana, biobancos y demás bancos de componentes anatómicos, de acuerdo con las competencias otorgadas para este fin.
CONSULTORSALUD pone a disposición de sus lectores este proyecto de decreto sobre componentes anatómicos para su lectura y análisis:
Le puede interesar: CONPES 4069: Política de ciencia, tecnología e innovación en Colombia