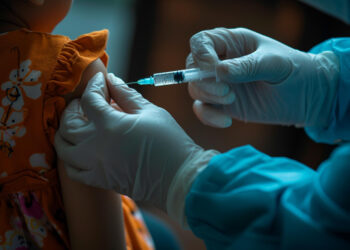
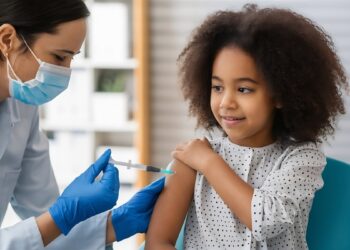
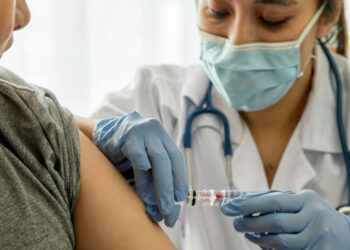
Con el Decreto 476 de 2020 se dictan nuevas medidas tendientes a garantizar la prevención, diagnóstico y tratamiento del COVID-19. Así mismo, se otorgan facultades transitorias al Invima y al Ministerio de salud, mientras dure la emergencia.
facultades al Ministerio de Salud y Protección Social
En primer lugar, el Ministerio de Salud podrá flexibilizar los requisitos para la evaluación de solicitudes de registro sanitario, los requisitos de fabricación, los requisitos de distribución y comercialización, así como, los permisos de comercialización o notificación sanitaria obligatoria, según corresponda, de medicamentos, productos fitoterapéuticos, dispositivos médicos, equipos biomédicos, reactivos de diagnóstico in vitro, cosméticos y productos de higiene doméstica y absorbentes de higiene personal que se requieran para la prevención, diagnóstico o tratamiento COVID-19.
Igualmente, el Ministerio de Salud podrá flexibilizar los requisitos para la habilitación del servicio farmacéutico en los establecimientos que se requieran, para la prevención, diagnóstico o tratamiento del Covid-19.
También puede leer: Se prohíbe a los empleadores obligar a tomar licencias no remuneradas
Del mismo modo, podrá declarar de interés en salud pública los medicamentos, dispositivos médicos, vacunas y otras tecnologías en salud que sean utilizadas para el diagnóstico, prevención y tratamiento del COVID-19
Finalmente, podrá establecer medidas para mitigar el eventual desabastecimiento de medicamentos, ocasionado por la cancelación o suspensión de la cadena de producción y comercialización a nivel mundial derivada de la pandemia COVID-19
facultades al Instituto Nacional de Vigilancia de Medicamentos y Alimentos -INVIMA
- Incorporar como vitales no disponibles aquellos medicamentos necesarios o relacionados con la prevención, diagnóstico y tratamiento del Covid- 19, o aquellos que se vean afectados por la cancelación o suspensión de la cadena de producción y comercialización a nivel mundial derivada de la pandemia Covid-19, sin necesidad de la verificación de desabastecimiento de medicamentos, dispositivos médicos y equipos biomédicos.
- Incorporar como vital no disponible aquellos reactivos de diagnóstico in vitro de metodología molecular en tiempo real (RT-PCR) para el diagnóstico de COVID-19 y otros reactivos avalados por la Organización Mundial de la Salud -OMS- u otras autoridades sanitarias, así como cosméticos, productos fitoterapéuticos y productos de higiene doméstica y absorbentes de higiene personal que se requieran para la prevención, diagnóstico y/o tratamiento del Covid- 19, o aquellos se vean afectados por la cancelación o suspensión de la cadena de producción y comercialización a nivel mundial derivada de la pandemia Covid-19, sin que sea necesario el concepto previo de la correspondiente Sala Especializada de la Comisión Revisora.
- Tramitar de manera prioritaria las solicitudes de registros sanitarios nuevos o permisos de comercialización y renovaciones de medicamentos que se encuentren en normas farmacológicas, productos fitoterapéuticos y dispositivos médicos, cuya clasificación de riesgo sea IIb y 111 que se requieran para la prevención, diagnóstico y/o tratamiento del Covid- 19, o aquellos determinados como de primera línea, accesorios o especiales
- Aceptar, homologar o convalidar las actas que concedan Buenas Prácticas de Manufactura (BPM) expedidas por agencias PIC-S (Pharmaceuticallnspection Co-operation Scheme), en los trámites de registro sanitario, renovaciones, modificaciones y trámites asociados, siempre y cuando sean aportadas en idioma españolo con su respectiva traducción, sin perjuicio de realizar la inspección, vigilancia y control posterior por parte de esa misma entidad.
-
 Suscripción Diamante$1.100.000 por 1 año
Suscripción Diamante$1.100.000 por 1 año -
 Suscripción ORO$350.000 por 1 año
Suscripción ORO$350.000 por 1 año -
 Suscripción plata$280.000 por 1 año
Suscripción plata$280.000 por 1 año -
 Suscripción gratuita$0 / año
Suscripción gratuita$0 / año